آیا میدانید که برخی ژنها میتوانند اثرات سایر ژنها را بپوشانند یا آنها را تغییر دهند؟ آیا این فرایند که اپیستازی نامیده میشود، میتواند کلیدی برای درک بیماریهای پیچیدهای مانند آلزایمر و دیابت باشد؟
مقاله مرتبط: جهشهای ژنتیکی یکسان، فنوتیپهای متفاوت؛ علت چیست؟
هنگامی که بحث در مورد فاکتورهای عامل بیماری است، معمولا وقوع جهشهای خاصی در یک ژن و یا فاکتورهای محیطی تاثیرگذار بر فنوتیپ بیماری به ذهن میرسند. موردی که علاوه بر اینها باید در نظر گرفته شود، اپیستازی است و فعل و انفعالات میان دو یا چند ژن را دربرمیگیرد. در واقع درک اپیستازی میتواند کلید درک بیماریهای پیچیدهای مانند آلزایمر، دیابت، بیماریهای قلبی-عروقی و سرطانها باشد.
اپیستازی تا چه حد در استعداد ابتلا به بیماریها موثر است؟
ارتباطات بین ژنی اپیستاتیک احتمالا شایعتر از آن چیزی هستند که تصور میشود. برخی از دانشمندان عقیده دارند که اپیستازی در بیولوژی به فراوانی رخ میدهد، در حالیکه در مطالعه صفات پیچیده از آنها چشمپوشی شده است. تحقیقات نشان داده است که ژنها به تنهایی عمل نمیکنند و به طور پیوسته با یکدیگر ارتباط دارند. این فعل و انفعالات بیولوژیکی در تنظیم ژنها، انتقال سیگنال، شبکههای بیوشیمیایی و انواع فراوان دیگری از مسیرهای فیزیولوژیکی و مربوط به رشد دارای نقش حیاتی هستند. فعل و انفعال برخی از ژنها با یکدیگر مثبت و برخی منفی است. در مجموع این ارتباطات منجر به فنوتیپ نهایی میگردند. ژنهای معینی فنوتیپ برخی از ژنهای دیگر را تغییر میدهند که منجر به تغییرات نفوذ و بیانپذیری ژنها میگردد.
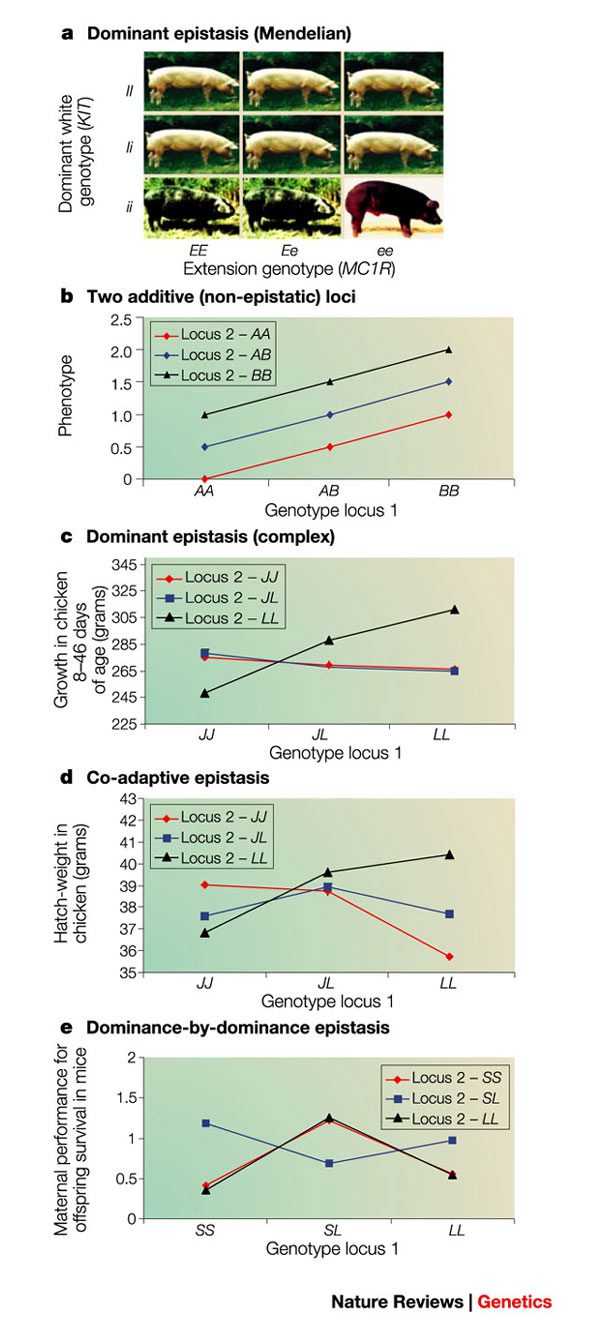
تاثیرات مربوط به اپیستازی میتوانند در مسیر مطالعه دانشمندان روی ژنهای مسئول بیماریهای پیچیده دشواری ایجاد کنند. به عناون مثال، در بسیاری از مطالعاتی که برای اولین بار روی ژنی درگیر در بیماری تمرکز کردهاند، با مطالعه تعداد افراد بیشتر، نتوانستهاند به طور کامل فنوتیپ بیماریهای پیچیده را توضیح دهند. این موضوع بیانگر آن است که چندین ژن درگیر هستند و فعل و انفعالات آنها به گونهای است که استعداد ابتلا به بیماریها را کاهش و یا افزایش میدهند. در صورتیکه تاثیر ژن عامل بیماری توسط ژن دومی پوشانده شده و یا تغییر داده شود، شناسایی ژن نخست دشوار خواهد بود. به علاوه، در صورتیکه بیش از یک ارتباط مربوط به اپیستازی باعث بیماری شود، شناسایی ژن درگیر و ارتباطات آن با سایر ژنها دشوارتر هم خواهد شد. البته روشهایی نیز به منظور مطالعه اپیستازی در جمعتی وجود دارد و با به کارگیری متدهایی انجام میشود که در شناسایی کمی لوکوسهای مربوط به صفت موردنظر استفاده میشود.
اپیستازی در بیماری آلزایمر
به منظور درک بهتر نحوه تاثیر اپیستازی بر توسعه بیماریها بهتر است نمونهای از یک بیماری پیچیده را بررسی کنیم. به عناون مثال، بیماری آلزایمر اختلال عصبی پیش روندهای است که باعث از دست رفتن حافظه و دمانس میگردد. در اوایل دهه ۱۹۹۰، تعدادی از دانشمندان دریافتند که ژنی به نام apolipoprotein E4 با ریسک بالای بیماری آلزایمر در ارتباط است. محققان همچنین عنوان کردند که علی رغم بالا رفتن ریسک ابتلا در صورت داشتن یک یا دو نسخه از این ژن، تمام افراد حامل یک یا دو نسخه از آن لزوما به بیماری مبتلا نمیشوند. این موضوع نشان میداد که در ابتلا به آلزایمر ژن یا ژنهای دیگری نیز دخیل هستند. درنتیجه Onofre Combarros و همکارانش مطالعهای را طراحی کردند تا نقش اپیستازی را در آغاز بیماری آلزایمر توضیح دهند. از آنجایی که پژوهشگران میدانستند مطالعه تک به تک ژنهای احتمالی، درصد موفقیت پایینی دارد، تیم تصمیم گرفت ارتباطات ژنی را بسنجد. در واقع Combarros و همکارانش به ارزشیابی میزان محتمل بودن حدود ۱۰۰ ارتباط اپیستاتیک منتشرشده در مورد بیماری آلزیمر پرداختند. برخی از این تاثیرات مربوط به اپیستازی در مورد چند جفت از ژنها مطرح شده بودند اما هرگز از لحاظ آماری سنجیده نشده بودند. در نتیجه به منظور ارزشیابی وقوع اپیستازی در هر یک از حالات، محققان به بررسی میزان ارتباطات و معناداری آماری میان جفت ژنهای مطرح شده پرداختند.
در نهایت، Combarros و همکارانش، ۲۷ ارتباط اپیستاتیکی مختلف را با استفاده از این متد اثبات کردند که در ۵ دسته قرار میگرفتند: متابولیسم کلسترول، تولید بتا آمیلوئید، التهاب، استرس اکسیداتیو و سایر موارد. برخی از این فعل و انفعالات سینرژیکی بوده و برخی دیگر آنتاگونیستی هستند. ارتباطات سینرژیکی نشاندهنده درگیر بودن جفتژنها در افزایش ریسک بیماری آلزایمر هستند. ارتباطات آنتگونیستی نیز نشانگر رابطه محافظتی بین دو ژن میباشند. قویترین ارتباطات میان جفتژنهای تشکبل شده میان آپولیپوپروتئین E4 با ۳ ژن مختلف مشاهده شد: alpha(1)-antichymotrypsin، β-secretase و butyrylcholinesterase K. در نتیجه واضح است که فعل و انفعالات اپیستاتیکی در بیماریهای پیچیدهای مانند بیماری آلزایمر دخیل میباشند و اینکه این ژنها به تنهایی تاثیر خود را اعمال نمیکنند، بلکه در مسیرهایی عمل میکنند که یکدیگر را تحت تاثیر قرار میدهند. در صورتی که اپیستازی در جمعیت بزرگتری از بیماران آلزایمری مطالعه میشد، ممکن بود بسیاری دیگر از فعل و انفعالات نیز از لحاظ آماری معنادار نشان داده شوند.
شواهد اپیستازی در سایر بیماریها
دیابت بیماری پیچیده دیگری است که تحت تاثیر هر دو عامل اپیستازی و فاکتورهای محیطی است. بیماری تنها در موارد نادر مونوژنیک است و معمولا چندین ژن درگیر هستند. در حالیکه میدانیم دیابتیها از وجود مقادیر ناکافی انسولین و قند خون بالا رنج میبرند، فاکتورهای زمینهای مستعدکننده به بیماری در حال بررسی هستند. به عنوان مثال، در مبتلایان به دیابت نوع ۲، فعل و انفعالات میان لوکوسهایی روی کروموزوم ۲ و ۱۵ و نیز بین لوکوسهایی روی کروموزوم ۱ و ۱۰ شناسایی شدهاند. ما امروزه هویت این ژنها را نمیدانیم، اما امیدواریم که در نهایت نقشهبرداری و شناسایی گردند. شواهد نشان میدهند که اپیستازی در بیماریهای پیچیده دیگری مانند بیماریهای قلبی عروقی، پرفشاری خون، اوتیسم، لب و/یا کام شکافدار، اسکیزوفرنی و سایر اختلالات نورولوژیکی و انواع سرطانها مانند سرطان سینه اسپورادیک، سرطان مثانه و سایر انواع سرطانها نقش دارد. درک عوامل و زمینه ژنتیکی در پس این بیماریها، در مطالعه ژنها به صورت تکی غیرممکن بود. در نتیجه محققان روی ارتباطات ژنتیکی بیشتر تمرکز کردند. در نتیجه پیشرفتهای بزرگتری به سمت درک تظاهرات این بیماریهای پیچیده در راه است.
امروزه شناسایی روابط ژنها، شبکههای ژنی و فعل و انفعالات اپیستاتیکی در سطح سیستمها در حال ممکن شدن است. امروزه، روشهای آزمایشگاهی پیشرفتهتری به منظور سنجش دادههای مولکولی و بیوشیمیایی در دسترس هستند. به عنوان مثال، DNA microarrayها این امکان را برای دانشمندان فراهم میکنند که صدها داده در سطح رونویسی (به عنوان فنوتیپ سنجیده شده) از سلولها جمعآوری شوند. متدهای محاسباتی و بیوانفورماتیک میتوانند در تحلیل و مرتبسازی حجم عظیم دادههای بیولوژیکی به منظور پیدا کردن روابط اپیستاتیکی مفید باشند. در صورت تعیین روابط اپیستاتیکی با استفاده از چنین تکنیکهایی قادر خواهیم بود، این دانش را در تشخیص و درمان بهتر بیماریهای پیچیده به کار بریم.
