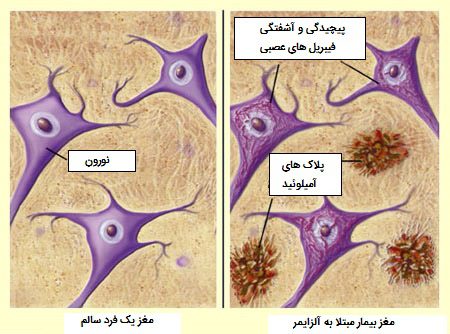
در عمق مغز ما جنگلی از ۱۰۰ میلیارد سلول عصبی وجود دارد. هر کدام از این سلولها دارای ۱۵۰۰۰ برآمدگی به نام دندریت هستند که در ارتباط با دندریتهای دیگر نورونها قرار میگیرند. بدین ترتیب بیش از ۱۰۰ میلیارد نقطه اتصال تشکیل میشود که در یک چشمبههمزدن حجم عظیمی از اطلاعات در آنها انتقال مییابد. سیگنالهای الکتریکی با سرعت ۲۰۰ بار در ثانیه از سلولی به سلولی دیگر منتقل شده و باعث ایجاد افکار، اعمال، خاطرات و احساسات ما میشود.
اما تصور کنید روزی ریشههای این جنگل پیچیده در همتنیده و ماده کثیف و چسبناکی در بین درختان ریخته شود. بدینترتیب فعالیت الکتریکی سلولها کاهش یافته و سلولها ضعیف شده و از بین میروند. درست همانند اکوسیستم فعالیکه خاموش میشود. میتوان گفت این همان چیزی است که در مغز بیمار مبتلا به آلزایمر اتفاق میافتد.
در آلزایمر چه اتفاقی میافتد؟
دانشمندان معتقدند پیچیدگی درون سلولها که tau tangles نامیده میشوند و پلاکهای پروتئینی آمیلوئید بین آنها، وضعیتی را ایجاد کردهاند که ۵.۵ میلیون آمریکایی را تحت تاثیر قرار داده است. با این حال علت دقیق این تغییرات هنوز یافت نشده است. از آنجا که هیچ راه مشخصی برای تایید تغییرات ایجاد شده در مغز وجود ندارد، پزشکان قادر به تشخیص قطعی این بیماری نیستند. به همین دلیل درحال حاضر پزشکان بیماران را با حذف سایر علل احتمالی علائمی شبیه زوال عقلی، تشخیص میدهند.
مقاله مرتبط: نزدیکترین دیدگاه در رابطه با پروتئینهای مرتبط با بیماری آلزایمر!
الماس و تشخیص آلزایمر
محققان به دنبال راهی برای تشخیص بیماری آلزایمر از طریق نشانگرهای زیستی یا همان بیومارکرها هستند. بیومارکرها اجسامی درون خون یا نمونههای بافتی هستند که ممکن است در هر بیماری خاصی ظاهر شوند. مطالعهای که اخیرا در ژورنال Proceedings of the National Academy of Sciences چاپ شده است، تکنیکی جدید به نام طیفسنجی ارتعاشی یا Vibrational spectroscopy را معرفی میکند و آن را امیدبخش میدانند. در طیفسنجی ارتعاشی با بازتاب نور از الماس، وجود بیومارکرهای مختص بیماری آلزایمر در خون تایید میشود. محققان گزارش دادند این تکنیک در مقایسه با تشخیصهای بالینی استاندارد (ترکیبی از سابقهی بیمار، آزمایشات فیزیکی و عصبی، تصویربرداریهای مغزی و غیره) موثرتر است.
هیجانانگیز ترین بخش آن این است که با این روش خون بیمار مبتلا به آلزایمر و بیمار مبتلا زوال عقل با اجسام لویی (LBD) از یکدیگر قابل تمیز هستند. اگرچه LBD دومین علت زوال عقل است ولی به علت تشابه علائم با دیگر اختلالات مغزی، اغلب به اشتباه تشخیص داده میشود. نکته مهم این است که یک تشخیص اشتباه ممکن است خطرناک باشد، زیرا ممکن است داروی خاصی که برای بیماری آلزایمر مفید شناخته شده است، بتواند عوارضی شدید مانند حساسیت نورولپتیک، پارکینسون برگشت ناپذیر یا سندرم بدخیم نورولپتیک ایجاد کند.
مقاله مرتبط: microRNA روشی پیشنهادی برای تشخیص زود هنگام آلزایمر
نقش PET در تشخیص آلزایمر
تحقیقات دکتر ون دیک پیشروی تکنیکهای در حال توسعه برای تشخیص آلزایمر از طریق بیومارکرها است. تیم او با همکاری مرکز تصویربرداری PET در بخش رادیولوژی پزشکی Yale، از تصویربرداری عصبی برای یافتن پروتئین آمیلوئید و تنگلهای تائو که از مشخصات بارز مغز بیماران مبتلا به آلزایمر هستند، استفاده کردند. بخش آمیلوئید این تکنیک در سال ۲۰۱۲ توسط FDA تایید شد. از آن زمان به بعد انقلابی در تحقیقات بالینی رخ داد؛ بطوریکه اسکن مثبت که نشاندهنده وجود آمیلوئید است لزوما به این معنی نیست که فرد آلزایمر دارد. از طرفی اسکن منفی به طور قطعی نشان میدهد که فرد آلزایمر ندارد. در حال حاضر، بسیاری از بیمارانی که قصد دارند در کارآزماییهای بالینی داروهای آلزایمر ثبت نام کنند، باید نتیجه مثبت از PET اسکن آمیلوئید را داشته باشند.
تصاویر PET به پزشکان این امکان را میدهد تا بیماری آلزایمر را زودتر از قبل تشخیص دهند. هرچقدر تشخیص آلزایمر سریع تر صورت بگیرد، پزشکان زودتر میتوانند داروهایی مانند مهارکننده های کولین استراز را که در بیماران مبتلا به آلزایمر خفیف تا متوسط کارآیی بیشتری دارد، تجویز کنند. این داروها از تشدید و پیشرفت بیماری از طریق مهار تجزیه استیل کولین توسط مغز جلوگیری میکنند. استیل کولین نقش مهمی در حافظه ایفا میکند. دکتر ون دیک میگوید:
آلزایمر باعث آسیب پیشرونده و غیرقابل بازگشت مغز میشود. هرچقدر زودتر به آن پی ببرید، مداخلات ما موثرتر خواهند بود.