زینک فینگر نوکلئازها۱، اندونوکلئازهای محدودکنندهی صناعی هستند که از دو دومین متصل شونده به DNA و برش DNA ساخته شدهاند. دومینهای زینک فینگر برای شناسایی توالی خاصی از DNA از میان کل ژنوم، طراحی میشوند.به کمک سیستم بازسازی DNA داخل سلولی ZFNها میتوانند با دقت بالایی ژنوم ارگانیسمهای تکامل یافته را تغییر دهند. به همراه کریسپر و TALEN، ZFN ابزار غالبی در زمینهویرایش ژنوم میباشد.
دومینها
دومین متصل شونده به DNA
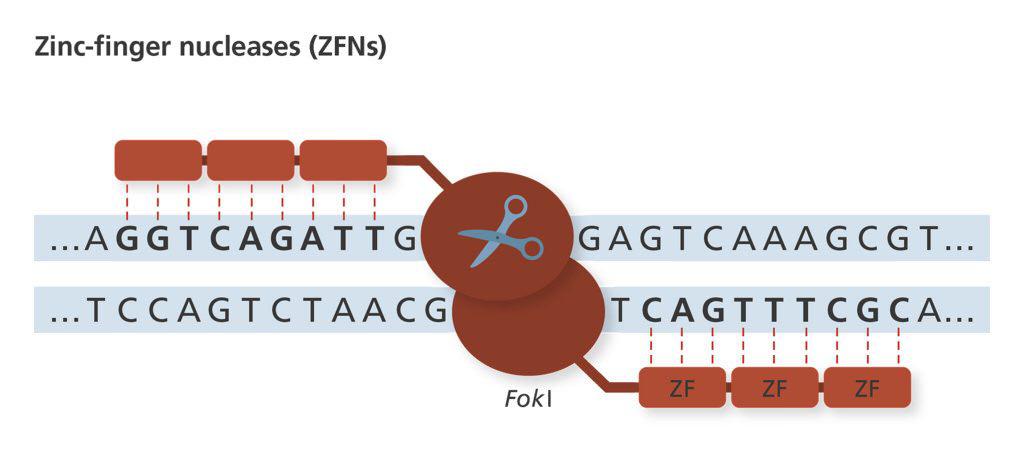
هر دومین زینک فینگر شامل ۳۰ اسیدآمینه است که دارای یک اتم روی میباشد که با دو اسیدآمینهی هیستدین و دو اسیدآمینه سیستئین پیوند غیرکووالان برقرار میکند. یک مارپیچ آلفا در هر دومین زینک فینگر سه جفت باز را شناسایی میکند. دومینهای متصل شونده هر ZFN به طور معمول شامل بین ۳ تا ۶ تکرار از زینک فینگر است، بدین ترتیب در یک دومین ۹ الی ۱۸ جفت باز شناسایی میشود. برای شناسایی موفقیتآمیز توالی DNA، هر زینک فینگر باید بتوانند با موفقیت توالی سه جفت باز را تشخیص داده و دومین زینک فینگر پشت سر هم قرار گرفته و جهتگیری مناسبی داشته باشند. مهمترین چالش پیش روی این فرآیند اختصاصیت هر زینک فینگر است که ممکن است با توالیهای شناسایی شده تسط سایر زینک فینگرها اشتراک داشته باشد و وابسته به محتوای توالی DNA و زینک فینگرهای اطرافش باشد (context dependence).
دومین برش DNA
دومین غیراختصاصی برش به طور معمول از اندونوکلئاز محدودکنندهی FokI تشکیل شده است. دومین نوکلئاز FokI به شکل دایمر عمل میکند؛ بنابراین برای برش ناحیه مورد نظر از DNA یک جفت ZFN مورد نیاز است تا ناحیه غیرمتقارنی از DNA را شناسایی کنند. در ZFNهای استاندارد، دومین برش به انتهای C-ترمینال هر دومین زینک فینگر متصل میشود. بدین ترتیب برای دایمر شدن دومینهای برش، هر ZFN باید به رشته مقابل DNA متصل شود.
 کاربردها
کاربردها
غیرفعال کردن یک الل
به کمک ZFNها میتوان موتاسیونهای غالب را در هتروزیگوتها غیرفعال کرد. در ناحیه مورد نظر، دو رشتهی DNA به کمک ZNFها شکسته میشود سپس در این ناحیه (در صورت عدم وجود الگوی همولوگ) توسط نوترکیبی غیرهمولوگ، ترمیم صورت میگیرد. در نوترکیبی غیرهمولوگ با به هم چسبیدن دو انتهای شکسته شده ترمیم رخ میدهد و درصورت بی نقص بودن برش هچگونه جهش ثانویه ایجاد نخواهد شد. اگرچه در برخی موارد ترمیم به درستی صورت نمیگیرد و سبب ایجاد حذف یا اضافه شدن جفت باز میشود، بدین ترتیب با ایجاد جهش دگرقالب تولید پروتئین معیوب متوقف میشود.
همچنین میتوان از ZNFهای چندگانه برای حذف یک بخش بزرگ از توالی ژنومی استفاده کرد. از ZNFها برای تغییر اللهای سهگانهی بیماریزا استفاده میشود. تکرارهای گستردهی CAG/CTG اساس بسیاری از بیماریهای ژنتیکی از جمله هانتینگتون، دیستروفی مایوتونیک و آتاکسیی هستند. مطالعات نشان دادهاند در سلولهای انسانی ZNFها میتوانند در تکرارهای CAG به طور مستقیم برش ایجاد کرده و اندازه توالی را از حالت طولانی و پاتولوژیک به حالت کوتاهتر که سمیت کمتری دارد تغییر دهند.
ویرایش اللها
ZNFها میتوانند با فعال سازی نوترکیبی همولوگ توالی یک الل را بازنویسی کنند. مکانیسم نوترکیبی همولوگ به دنبال توالی همسان میان کروموزم آسیب دیده و قطعهی خارج کروموزومی گشته و بدون توجه به اینکه قطعه حاوی توالی اصلی میباشد یا نه، آن را بین دو انتهای شکسته شده (توسط ZNF) کرومزوم کپی میکند. درصورت همزیگوت بودن سلول اثرگذاری این تکنیک کاهش مییابد؛ زیرا ممکن است به جای قطعهی خارجی کپی دستنخوردهی الل به عنوان الگویی برای ترمیم استفاده شود.
مشکلات بالقوه
برشهای نا به جا
اگر دومینهای زینک فینگر برای شناسایی توالی هدف به اندازه کافی اختصاصی عمل نکرده و یا بیش از یک ناحیه را در ژنوم شناسایی کنند، برش نه به جا (off-target cleavage) رخ خواهد داد. این برش نه به جا به اندازهای در طول DNA شکستها دو رشتهای ایجاد میکند و سیستم ترمیم سلولی بیش از اندازه به کار گرفته میشود. در نتیجهی بازآرایی متعدد کروموزومی مرگ سلول رخ میدهد. برش نا به جا همچنین ممکن است موجب ادغام تصادفی DNA خارجی به درون کروموزومها شود.
ایمنوژنسیته
همانند هر پروتئین خارجی تزریق شده به داخل بدن انسان، ریسک بروز پاسخ ایمنی علیه عوامل درمانی و سلولهای حاوی آنها وجود دارد. اگرچه به دلیل بیان گذرای پروتئینهای اندونوکلئاز احتمال رخ دادن پاسخ ایمنی در این فاصله کوتاه زمانی کم است.
۱. نوکلئازهای انگشت روی؛ که به دلیل شکل خاص پروتئین و حضور عنصر روی، به این نام نامیده شدهاند.

 کاربردها
کاربردها