نقایص مادرزادی علت عمدهی مرگ ومیر نوزادان در سراسر جهان به شمار میروند. آنها هم که در کودکی جان سالم به در میبرند، اغلب تمام طول عمر خود را با ناتوانیهای ذهنی و فیزیکی سپری میکنند. آیا میتوانیم از این وضعیت پیشگیری کنیم؟
نقایص مادرزادی علت عمدهی مرگ ومیر نوزادان در سراسر جهان به شمار میروند. آنها هم که در کودکی جان سالم به در میبرند، اغلب تمام طول عمر خود را با ناتوانیهای ذهنی و فیزیکی سپری میکنند. نقایص مادرزادی از علل متعددی ناشی میشوند. برخی نقایص ژنتیکیاند، برخی تحت تأثیر فاکتورهای محیطی بوده و برخی دیگر نیز تحت تأثیر ترکیب ژنتیک و محیط میباشند. اما آیا میتوان برای کاهش بروز و محدود کردن اثرات نقایص مادرزادی کاری کرد؟ در برخی موارد -خصوصاً آنهایی که موروثی هستند- پاسخ منفی است. با این حال در موارد دیگر، فاکتورهایی همچون مطلوب بودن محیط قبل از تولد و درمان زودهنگام میتوانند از اثرات فنوتیپی نقایص مادرزادی، از جمله نقایصی که اساس ژنتیکی دارند، پیشگیری کرده یا آنها را کاهش دهند.
پیشگیری و محیط قبل از تولد
چنانچه اشاره شد، درصد قابل توجهی از نقایص مادرزادی به طور کامل یا نسبی در اثر فاکتورهای محیطی رخ میدهند. مهمترین فاکتورها در این ارتباط آنهایی هستند که بدن زن را قبل از حاملگی یا طی آن تحت تأثیر قرار میدهند؛ چرا که بدن زن، اساس محیط قبل از تولد کودک را تشکیل میدهد. از این رو راهکارهایی که این محیط را مطلوبتر سازند، در کاهش اثرات برخی از انواع نقایص مادرزادی مؤثر خواهند بود.
افزایش مصرف فولیک اسید
یکی از مثالها در مورد تلاشهای مؤفقی که در راستای تغییر محیط قبل از تولد صورت گرفته است، غنیسازی منابع غذایی ایالات متحده با یک نوع ویتامین B تحت عنوان فولیک اسید است. خدمات سلامت عمومی ایالات متحده در سال ۱۹۹۲ توصیه کرد تمامی زنانی که در سنین باروری قرار دارند، روزانه ۴۰۰ میکروگرم از این ویتامین را مصرف کنند (مطالعهی محقق Blom در سال ۲۰۰۶). فولیک اسید فرم مصنوعی ویتامین فولات است که در بسیاری از غذاها، خصوصاً با غلظت بالا در سبزیجات دارای برگهای سبز، وجود دارد. به طور طبیعی حدود ۲۸ امین روز پس از لقاح، سلولهای مسئول تکامل سیستم عصبی جنین، به منظور تشکیل لولهی عصبی تا میخورند. این لوله در ادامهی تکامل خود مغز و طناب نخاعی را ایجاد خواهد کرد (تصویر ۱). به هر حال، کمبود میزان فولیک اسید مادری با نقایص لولهی عصبی در جنین در حال تکامل ارتباط دارد (مطالعهی محقق Smithells در سال ۱۹۷۶)؛ اما اگر فولیک اسید در مراحل اولیهی بارداری مصرف گردد، خطر نقایص مادرزادی مغز و طناب نخاعی کاهش مییابد (مطالعات محقق Blom و همکارانش، ۲۰۰۶؛ محقق Smithells در سال ۱۹۸۱؛ محقق Smithells در سال ۱۹۸۳؛ محقق Laurence در سال ۱۹۸۱).
دیده شده است که مصرف مکملهای فولیک اسید، تقریباً از ۵۰ تا ۷۵ درصد از نقایص لولهی عصبی پیشگیری میکند. با این وجود، علیرغم ارتباطی که میان فولیک اسید و نقایص مادرزادی وجود دارد، زنان اغلب طی ۲۸ روز اول حاملگی خود فولیک اسید کافی مصرف نمیکنند. در واقع، بسیاری از زنان زمانی در این خصوص آموزش میبینند که لولهی عصبی جنینشان تقریباً به طور کامل بسته شده است. بر این اساس در سال ۱۹۹۸ در راستای مقابله با این مسئله، دولت ایالات متحده غنیسازی آرد و سایر غلات با فولیک اسید را اجباری کرد. از آن زمان بروز نقایص لولهی عصبی در متولدین این کشور به میزان ۱۹ درصد کاهش یافته است (مطالعهی محقق Blom در سال ۲۰۰۶).
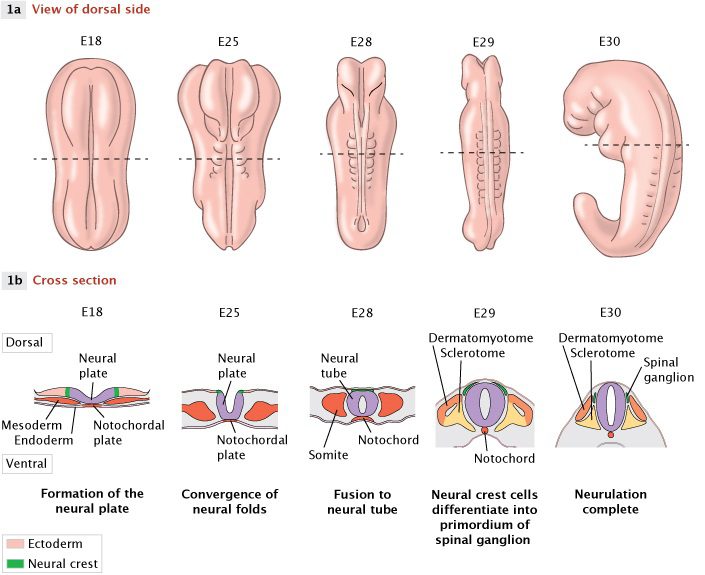
تصویر ۱: مراحل اصلی بسته شدن لولهی عصبی
در جنین در حال تکامل انسان، بسته شدن لولهی عصبی شامل سه مرحلهی اصلی است که این سه مرحله در تمامی پستانداران مشترک هستند. اگر لولهی عصبی نتواند به طور کامل در طول شکاف پشتی بسته شود، اسپاینا بیفیدا رخ میدهد. در این تصویر، از چپ به راست، تکامل جنین از روز ۱۸ ام (E18) به بعد نشان داده شده است. در ردیف ۱a نمای پشتی جنینِ کامل دیده میشود. در ردیف ۱b نیز برش مقطعی از بافت زیرین مشاهده میشود که این برش در طول نقطهچین افقی موجود در ردیف ۱a تهیه شده است. تقریباً از حوالی روز هجدهم (E18)، چینهای عصبی طی فرآیندی به نام ترکیب دو سویه (bidirectional fusion) به طرف داخل کشیده میشوند. این فرآیند یک فرورفتگی تحت عنوان شیار عصبی (neural groove) در صفحهی عصبی ایجاد میکند. در نهایت صفحهی عصبی در سمت پشتی از دو جهت به هم رسیده و ترکیب میشود. نتیجهی این امر، ایجاد ساختمانی توخالی به نام لولهی عصبی است ( ردیف ۱b به رنگ بنفش). فضای توخالی در نهایت کانال مرکزی نخاع تکامل یافته را تشکیل میدهد. این فرآیند تشکیل لوله، محور بدن را در طول نخاع قرار داده و ساختار سیستم عصبی محیطی را که از آن رشد خواهد یافت، تعیین میکند. در عین حال که لوله تشکیل شده و بسته میشود، برخی سلولهای مشتق شده از صفحهی عصبی وجود دارند که به جای قرار گرفتن در خود لوله، بالای آن استقرار می یابند. این سلولها (به رنگ سبز)، سلولهای ستیغ عصبی نامیده میشوند که در ادامه با مهاجرت، بافتهای محیطی مختلفی را در بدن تشکیل میدهند. لولهی عصبی در مجاورت سومایتها واقع شده که نهایتاً قفسهی سینه، استخوانها و عضلات را ایجاد میکنند. در سطح شکمی لولهی عصبی ساختار مهمی به نام نوتوکورد وجود دارد که به تعیین محور طولی بدن حین تکامل اولیه کمک میکند. بسته شدن لولهی عصبی در حالت طبیعی تا روز ۳۰ ام (E30) کامل میشود.
کاهش مصرف قند
چنانچه مثال فولیک اسید نشان میدهد، تعادل درست مواد مغذی قبل از تولد، فاکتور محیطی کلیدی در تکامل کودک سالم است. اگرچه کمبودهای تغذیهای میتوانند پیامدهای زیانباری داشته باشند، مصرف مازاد برخی مواد همچون قند نیز میتواند با اثرات منفی همراه باشد. به عنوان مثال، دیابت بارداری میتواند در زنان بارداری که هیچ نوع سابقهی دیابت ندارند، رخ دهد. در زن باردار ممکن است به علت تغییرات هورمونی مرتبط با تشکیل جفت، مقاومت به انسولین ایجاد شود (مطالعهی محققان Buchanan و Xiang در سال ۲۰۰۵). زنان باردار را میتوان از نظر دیابت بارداری غربالگری کرده و در صورت ابتلا، با ورزش و محدود ساختن مصرف قند، بیماری را کنترل کرد. دیابت بارداری همچنین میتواند خطراتی برای نوزاد داشته باشد. این نوزادان ممکن است به صورت نارس با وزن بیشتر یا کمتر از حالت طبیعی متولد شوند. همچنین این کودکان پس از تولد ممکن است اختلالات رشدی داشته باشند. خطر چاقی در کودکی و بزرگسالی نیز برایشان بیشتر است (مطالعهی محقق Boney در سال ۲۰۰۵؛ محقق Whitaker در سال ۱۹۹۸). خطر مشکلات تنفسی نیز در نوزادان نارس بالاتر است؛ چرا که ریههای این نوزادان به طور کامل تکامل نیافتهاند. علاوه بر این، در مادرانی که دیابت بارداری داشتهاند، خطر بروز دیابت پس از حاملگی، بیشتر است (مطالعهی محققان Buchanan و Xiang در سال ۲۰۰۵).
محدود ساختن مواجهه با تراتوژنها و جهشزاها
علیرغم شناسایی بسیاری از کمبودهای تغذیهای که اثر منفی بر محیط قبل از تولد دارند، گسترهی حقیقی اثرات تغذیه همچنان حوزهای فعال در تحقیقات محسوب میشود. به طور مشابه، مطالعه در مورد اثرات دقیق تراتوژنها و جهشزاهای مختلف بر تکامل جنین، همچنان ادامه دارد.
هر مادهای که مشخص شود موجب نقایص مادرزادی در انسان میگردد، تراتوژن نامیده میشود. از جمله مثالهای رایج میتوان به الکل، دود سیگار، داروهای خاص و مواد شیمیایی صنعتی بیشمار اشاره کرد. این مواد با ایجاد تغییر در محیط واقعی داخل رحم، باعث بروز نقایص مادرزادی میشوند. به عنوان مثال، افزایش سطح نیکوتین متعاقب استعمال دخانیات در دورهی حاملگی با افزایش خطر تولد نوزاد مرده، تولد نوزاد کموزن و بروز لب یا کام شکافدار ارتباط دارد. به طور مشابه، الکل را نیز میتوان جزو تراتوژنها طبقهبندی کرد؛ چون مصرف این ماده در دورهی حاملگی ممکن است به نقص عضو جنین، ویژگیهای غیرطبیعی صورت، عقبماندگی ذهنی و مشکلاتی دیگر منتج شود.
دقیقاً به همان میزان که مواجهه با تراتوژنها حین بارداری میتواند آثار زیانبار داشته باشد، مواجههی مادر با جهشزاها حتی قبل از لقاح نیز با چنین اثراتی همراه است. به طور ساده جهشزا مادهای است که ساختار مادهی ژنتیک سلول را تغییر میدهد. از این رو، اگر زنی حتی قبل از باردار شدن با مادهای جهشزا مواجهه داشته و این ماده DNA یک یا بیش از یکی از سلولهای زایا را تغییر دهد، این امر تأثیر منفی بر نوزاد آینده خواهد داشت. جهشزاها از مواد شیمیایی گرفته تا اشعههای یونیزان، انواع مختلفی دارند. تعدادی از تراتوژنهای رایج از قبیل دود سیگار و الکل نیز میتوانند اثر جهشزایی داشته باشند. بدان جهت محدود ساختن مواجهه با تراتوژنها و جهشزاها هم قبل از حاملگی و هم حین حاملگی، یکی از فاکتورهای اصلی محیطی است که در کنترل زن میباشد.
تشخیص و درمان زودهنگام بیماریهای مادرزادی
بسیاری از بیماریهای مادرزادی قابل پیشگیری نیستند؛ خصوصاً مواردی که اساس ژنتیکی دارند. اما خوشبختانه با روشهای غربالگری و درمان موجود، میتوان از عوارض بیماریهای مادرزادی جلوگیری کرده و شانس زندگیِ با کیفیت بهتر را برای کودکان مبتلا افزایش داد. به عنوان مثال، برای تشخیص آنومالیهای جدی جنینی از جمله نقایص لولهی عصبی و اختلالات کرومووزومی، میتوان از اولتراسونوگرافی و آنالیز سرم مادری استفاده کرد. به علاوه، پس از تولد میتوان نوزادان را از نظر اختلالات ژنتیکی، هماتولوژیکی، متابولیکی و هورمونی مختلف غربالگری کرد تا در صورت وجود ناهنجاری، تشخیص زودهنگام صورت گیرد.
تشخیص و درمان زودهنگام نقایص مادزادی میتواند به پیشگیری از تولد نوزادان مرده یا پیشگیری از بروز ناتوانیهای فیزیکی و ذهنی کمک کند. برای نمونه اختلال شنیداری مادرزادی را در نظر بگیرید که میتواند ناشی از علل ژنتیکی یا محیطی متعدد باشد. در صورت عدم بررسی زودهنگام، تشخیص ناشنوایی ممکن است به دو یا سه سالگی کودک موکول گردد؛ زمانی که تأخیر در گفتار و تکامل زبانی نمایان میشود. مثال دیگر در این باره فنیل کتونوری است. این بیماری اختلالی موروثی است که با عدم امکان ساخت آمینواسید تیروزین از فنیلآلانین شناخته میشود. درمان این بیماری تجویز رژیم غذایی محتوی فنیلآلانین کم و تیروزین زیاد است که شروع درمان از همان زمان تولد، نتایج بسیار خوبی دارد.
برای درمان بسیاری از نقایص مادرزادی مانند لب و کام شکافدار و اسپایندا بیفیدا، میتوان جراحی انجام داد؛ حتی گاهی جراحی قبل از تولد نیز صورت میگیرد. هدف از جراحی قبل از تولد، محدود ساختن آسیبهای درازمدت از طریق مداخلهی زودهنگام است. نقایص قبل از تولدِ قلبی و سیستم کلیوی اغلب در عین حال که جنین در رحم قرار دارد، با جراحی درمان میشوند. این امر با کاستن فشار و تصحیح زودهنگام نقص موجود، امکان پیشآگهی تکاملی بهتر را فراهم میکند. در آخر، اگرچه ژندرمانی نیز گزینهای امکانپذیر برای درمان برخی بیماریهای ژنتیکی است، اما هنوز در مقیاس گسترده مورد استفاده قرار نگرفته است.