فعالیت گروهی لزوماً باعث نمیشود که یک پروتئین کشنده باشد. این تجمع پروتئینی فقط تحت شرایط خاصی به عوارض خطرناک ختم میشود.
یک پروتئین بیضرر میتواند به گونهای مهندسی شود تا با ظاهرسازی رفتاری مشابه پروتئینهای بیماریزا، تودههای پروتئینی در بدن تشکیل دهد؛ حالتی که منجر به بروز بیماریهایی نظیر آلزایمر، پارکینسون و جنون گاوی (CJD، بیماری کروتزفلد-یاکوب، نوعی بیماری تحلیل برندۀ مغز که تحت تأثیر پریونها ایجاد میشود) میشود. در نتیجۀ این تجمع، سلولهایی که برای زنده ماندن به فعالیت صحیح این پروتئینها نیاز دارند از بین میروند. با این حال محققان دریافتهاند که سلولهایی که به این پروتئینها نیازی ندارند هیچگونه آسیبی دریافت نمیکنند. این یافته میتواند به تشریح این سؤال مهم که “چرا پروتئینهای تجمعی دخیل در بیماریهای تخریبکنندۀ معز، گروهی از سلولها را تخریب کرده اما به انواع دیگر آسیبی نمیرسانند؟” کمک کند.
دانشمندان همچنان علت این رفتار تهاجمی و چگونگی انجام آن را (که به تخریب سلولی میانجامد) به شکل واضح درک نکردهاند. بخشی از علت دشواری بازسازی این فرآیند به این دلیل است که محققان هنوز کارکرد [احتمالی] بسیاری از پروتئینها را شناسایی نکردهاند.
اخیراْ تیمی از پژوهشگران به رهبری فردریک روسو (Frederic Rousseau) و جوست شایمکوویتز (Joost Schymkowitz) از دانشگاه کاتولیک لوون بلژیک (Katholieke Universiteit Leuven) به روش جدیدی جهت تشریح پروتئینها دست یافتهاند. در این روش پروتئینی با کارکرد شناخته شده به گونهای مهندسی میشود تا فعالیت تجمعی پیدا کند. این پروتئین، VEGFR2 یا گیرندۀ شماره ۲ فاکتور رشد سلولهای پوششی عروقی (Vascular Endothelial Growth Factor Receptor 2)، موجب رشد عروق خونی میشود. روسو و همکارانش با برش بخشی از این پروتئین که منجر به بروز خاصیت تجمعی در آن میشود، موفق به ساخت یک آمیلویید مصنوعی شدند.
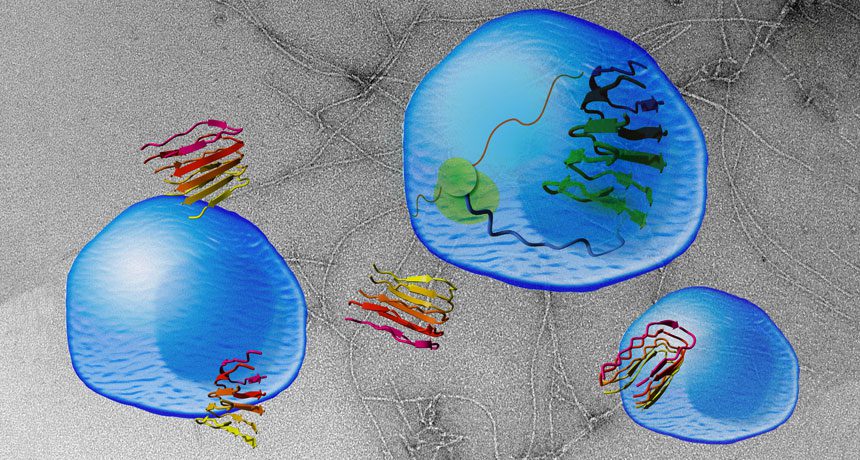
این قطعات پروتئین موسوم به واسین (Vascin) میتوانند با تجمع و تشکیل تودههای پروتئینی فعالیت طبیعی VEGFR2 را مهار کنند. زمانی که واسین به محیط کشت سلولهای ورید نافی (Umbilical) اضافه شد، سلولها مردند؛ چرا که با مهار فعالیت VEGFR2، سیگنالهای هورمونی ضروری برای زنده ماندن سلولها نیز دیگر منتقل نمیشدند. ولی سلولهای کلیوی رویان و سلولهای سرطانی استخوان انسان هنگامی که در معرض واسین قرار گرفتند، هیچگونه آسیبی دریافت نکردند. این مشاهدهها میتواند بدین معنی باشد که آمیلوییدها ذاتاً برای سلول سمی نیستند؛ بلکه با تغییر فعالیت پروتئینهای خاصی که برای زنده ماندن سلول ضروری است، اثرات آسیبزای خود را اعمال میکنند.
این یافتهها همچنین میتوانند تخریب سلولهای مغزی ناشی از بتا-آمیلوییدها در طی بیماری پارکینسون را تفسیر کند؛ چرا که این دسته از آمیلوییدها نقش مهمی در کارکرد سلولهای آسیبپذیر مغزی دارند.
احتمالاً در آینده بتوان از این دست پروتئینهای مهندسی شده برای کنترل کارکرد پروتئینهای دخیل در بیماریهایی نظیر سرطان بهره برد. برای نمونه؛ آمیلوییدهای مصنوعی مهارکندۀ پروتئینهای بیشفعال (Overactivated) در بیماری سرطان؛ با القای اثر تجمعی و تشکیل توده میتوانند این قبیل از پروتئینها را از کار بیندازند.
