الکل یکی از شناخته شدهترین عوامل تخریب اندامهای بدن است که تأثیرات جدی آن بر سلامت ثابت شده است. از خیلی وقتها پیش تأثیرات اجتماعی آن نیز مشاهده شده و همچنان هم میشود! همچنین یک عامل ازبین برندهی شناختهشدهی سلول است که از راههای زیادی باعث آسیب عصبی میشود. با وجود اینکه مطالعات زیادی در این باره انجام شده است ولی مکانیسم دقیق آن هنوز مشخص نیست. سلولهای عصبی به طور عمده در دو ناحیه از سیستم عصبی از سلولهای بنیادی به وجود میآیند؛ یکی در ناحیهی subventricular (زیربطنی) و دیگری در dentate gyrus که در هیپوکامپ قرار دارد. این سلولها توانایی تبدیل به سلولهای عصبی و غیرعصبی مغز و نخاع را دارند. مطالعات جدید از دخالت این سلولها در انواع ناهنجاریهای عصبی خبر میدهد.
مصرف زیاد الکل روند ایجاد سلولهای عصبی از سلولهای بنیادی را با مشکل روبهرو میکند. این مشکل در آزمایشگاه هم مشاهده شده است. این یافتهها احتمال ارتباط بین این اختلال و مرگ سلولهای عصبی را بیشتر میکند. تولید سلولهای عصبی (نوروژنسیس) را میتوان در چهار مرحله مطالعه کرد: تکثیر، مهاجرت، تمایز و ابقاء سلولها. مطالعات، تأثیر الکل را در مرحله تمایز نشان میدهد که در آن عامل محدودکننده نورونی رونویسی را در سلولهای عصبی با مشکل مواجه میکند.
تخمین زده میشود که ۱۴۰ میلیون نفر در سراسر جهان دچار الکولیسم باشند. الکولیسم به عدم توانایی کنترول مصرف الکل در افراد گفته میشود که به دلیل وابستگی جسمی و روانی ایجاد شده توسط آن به وجود میآید.
این عقیده که سلولهای عصبی نمیتوانند در انسانهای بالغ به وجود بیایند با تحقیقاتی که توسط Reynolds and Weiss انجام شد، دیگر اعتبار خود را از دست داد. این محققان موفق شدند سلولهایی را در سیستم عصبی مغز موشها تحریک به تقسیم کنند. سرانجام هم تکثیر سلولهای بنیادی و تبدیل آنها به نورون مستقیماً مشاهده شد. این فرآیند در همه پستاندارن مثل انسان مشاهده میشود. ارتباط این پژوهشها با هم از نقش این یافتهها در ناهنجاریهای وابسته به الکولیسم خبر میدهند.
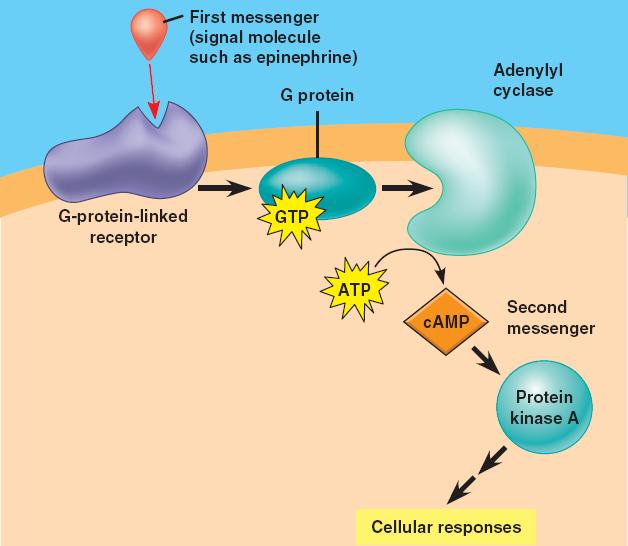
مصرف الکل نوعی پاداش برای مغز تلقی میشود و نوعی حس رضایتمندی و وابستگی را در انسان القاء میکند. مصرف دائمی الکل به سیستم پیامرسانی داخل سلولی نورونها آسیب میرساند. بررسی سلولهای عصبی پس از مرگ نشان میدهد که در آنها آدنیلیل سیکلاز کاهش مییابد. این پروتئین در ایجاد cAMP که پروتئین کیناز را فعال میکند نقش دارد. پروتئین کیناز به هسته رفته و با فسفوریلاسیون یک عامل رونویسی از بیان برخی ژنها جلوگیری میکند. یکی از این ژنها برای سنتز انتقالدهندههای عصبی و مولکولهای ضروری برای بقای نورون، لازم است.
سلولهای بنیادی به دلیل خاصیت تبدیل خود به سلولهای مختلف توجه محققان را به خود جلب کرده است، از جمله نقش آنها در ناهنجاریهای عصبی. همچنین در این ناهنجاریها مثل افسردگی و… حجم هیپوکامپ نیز کاهش مییابد. در روشهای درمانی که برای این بیماریها به کار میرود میزان تکثیر سلولهای بنیادی عصبی افزایش مییابد.
آسیبی که مصرف الکل به سیستم عصبی میرساند هم به نورونهای بالغ اثر میکند هم به نورونهایی که در حال تکوین هستند. این کار با فعال کردن مسیرهای مرگ سلولی (آپوپتوز) در سلولهای بالغ و طولانی کردن چرخه سلولی در سلولهای بنیادی، مخصوصاً در مرحله تمایز انجام میگیرد. انهدام چند سلول آسیب خاصی نمیرساند ولی وقتی این مقدار بیشتر شود بخشی از شبکه عصبی ناقص میشود.
نوزادانی که از مادرانِ با سابقه مصرف سنگین الکل به دنیا میآیند ممکن است مجموعهای از نشانههای عصبی را نشان دهند که در مجموع به آن “اثر کشنده الکل” میگویند. این اثر منجر به ایجاد عقبماندگیهای پیش و پس از تولد نیز میشود. دلیل این اثر هم تأثیر مخرب بیشتر الکل روی مغز در حال تکامل است تا مغز تکاملیافته!
اکنون کار روی سلولهای بنیادی دو دسته شده است؛ عدهای سعی دارند مسیرهای تخریب آنها را بفهمند و عدهای در تلاش اند تا با استفاده از آنها در درمان بیماریهایی مثل آلزایمر، پارکینسون و… پیشرفت حاصل کنند ولی هنوز درمان قابل ملاحظهای با این روش روی سلولهای عصبی پیدا نشده است.
با وجود هزاران مطالعات انجام شده در این زمینه، دلیل اصلی تأثیر الکل روی سلولهای عصبی هنوز کاملاً مشخص نشده است. نقش سلولهای بنیادی عصبی در این زمینه جزو آخرین یافتههاست و دانشمندان امیدوارند تا این یافتهها درهای جدیدی را به رویشان باز کند.
منبع: ncbi