فیزیکدان و شیمیدان بریتانیایی، رابرت بویل (Robert Boyle)، از چهرههای علمی سرشناس در زمان خود بود و امروزه به عنوان یکی از بنیانگذاران شیمی مدرن محسوب میشود. عمده شهرت بویل مربوط به تئوری بسیار مطرحی در زمینه گازهاست که تحت عنوان قانون بویل (Boyle’s Law) شناخته میشود.
نام دستاورد: قانون بویل
تاریخ انتشار: ۱۶۶۲
ارائهدهنده: رابرت بویل (Robert Boyle)
بر اساس قانون بویل اگر حجم گازی کاهش یابد، فشار متناسب با آن افزایش پیدا خواهد کرد. رابرت بویل با بیان این که تمامی گازها از ذرات بسیار ریزی ساخته شدهاند، سعی داشت نوعی تئوری ذرهای برای آن پایه گذاری نماید که در سراسر دنیا به کار گرفته شود. علاوه بر آن، وی توانست معنای جدیدی به مفهوم “عنصر” ببخشد و تست لیتموس (litmus test) را جهت مشخص نمودن میزان بازی و یا اسیدی بودن مایعات طراحی نماید.
بویل آموزشهای مقدماتی را در ایتن (Eaton) فرا گرفت و سپس برای ادامۀ تحصیل – در قالب دورههای آموزشی خصوصی – به ژنو سوئیس فرستاده شد. او در ۱۲ سالگی، پیش از آن که در ژنو مستقر شود، تمامی اروپا را گشته بود. دروسی که وی در این دوره فراگرفت شامل زبانهای فرانسوی و لاتین، بلاغت (rhetoric)، فقه و از همه مهمتر، ریاضیات، میشده است.
بویل با عطشی مضاعف برای یادگیری به خانۀ خود بازگشت. از دیدگاه وی هنوز جوانب بسیار زیادی از عالم طبیعت توضیح داده نشده بود و پتانسیل این را داشت که در قالب مجموعهای از قوانینی ریاضی تعریف شود.
رابرت بویل در سال ۱۶۶۰ به همراه ۱۱ چهرۀ سرشناس دیگر انجمن سلطنتی لندن را تأسیس نمود. نام کامل انجمن مذکور Royal Society of London for Improvement of Natural Knowledge میباشد و همانطور که از بر میآید، با هدف اعتلای سطح دانش بشر از علوم طبیعی پایهگذاری شده است.
بویل در اواسط قرن هفدهم به آکسفورد نقل مکان کرد. وی در آنجا دستیاری برای خود برگزید، که رابرت هوک (Robert Hooke) نام داشت. آن دو به کمک هم توانستند نمونهای اولیه از اتاقک خلأ (vacuum chamber) یا همان پمپ هوا بسازند.
رابرت بویل و رابرت هوک از پیشگامان عصر خود محسوب میشدند. این دو به جای رسانهای ساختن کشف خود و بهرهگیری از منطق و فلسفه ارسطویی به منظور اثبات کردن آن، ترجیح دادند به مشاهده مستقیم در طبیعت پرداخته و بر اساس این مشاهدات ثبت شده نتیجهگیری نمایند.
بویل یکی از اولین دانشمندانی بود که در آزمایشهای خود از نمونههای کنترل (شاهد) نیز استفاده کرد. او نتایج کار خود را به عنوان مرجعی جهت استفادۀ دیگر پژوهشگران منتشر نمود که در آن به شرح جزء به جزء مراحل انجام آزمایش، دستگاههای به کار برده شده و مشاهدات صورت گرفته پرداخته بود. وی در چندین رشته، از جمله فلسفه، پزشکی و فقه صاحبنظر بود و کتاب شیمی دان شکاک (Sceptical Chymist) خود را نیز در سال ۱۶۶۱ منتشر کرد که در آن تئوری عناصر چهارگانه ارسطو را مورد انتقاد قرار داده بود. این اقدام به شکلگیری تئوری مدرن عناصر شیمیایی انجامید.
گزارۀ “در دمای ثابت، فشار گاز با حجم آن رابطۀ عکس دارد” که در سراسر دنیا به عنوان قانون بویل شناخته میشود، در سال ۱۶۶۲ ضمیمیۀ یکی از کتابهای بویل به نام New Experiments Physico-Mechanicall, Touching the Spring of the Air and its Effects گردید. این کتاب در سال ۱۶۶۰ منتشر شده بود. اتاقک خلأ دستاورد سه سال همکاری بویل با هوک میباشد. اتاقک خلأ یا پمپ هوا توسط هوک ساخته شد و از بویل از آن در مطالعات خود استفاده میکرد. او با همین دستگاه توانست به چندین کشف مهم دست یابد:
- صوت در خلأ منتشر نمیشود.
- سوختن در حضور هوا صورت میگیرد.
- و همچنین چندین مشاهده در خصوص ویژگیهای الاستیک هوا
بسیاری از دانشمندان در آن دوره امکان وجود خلأ را باور نداشتند، که بویل را مجبور کرد برای اثبات وجود آن ضمیمهای را در سال ۱۶۶۲ به عنوان مدرک به کتاب خود اضافه کند. برای مثال، دکارت به وجود “اتر تماماً فراگیر” (all-pervading ether) اعتقاد داشت. بویل با این که تئوری دکارت را به دلیل عدم برخورداری از شواهد علمی کافی نقض نمود، ولی موافق این قضیه بود که “جهان اساساً سیستمی پیچیده است که توسط تعدادی از قوانین کوچک ریاضی هدایت میشود”.
قانون بویل
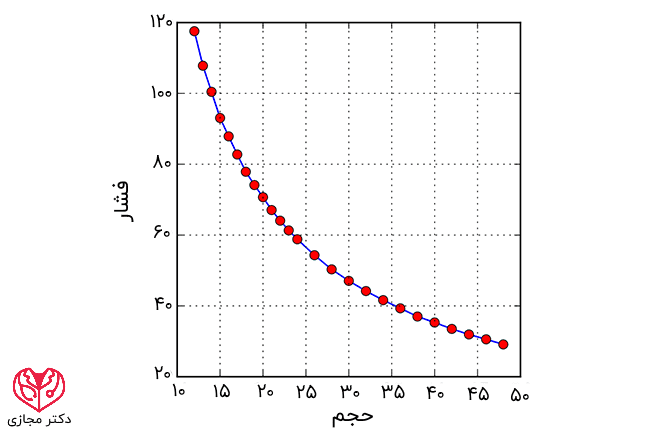
رابرت بویل در سال ۱۶۶۲ قانونی را توصیف نمود که پیش از آن توسط ریچارد تاونلی (Richard Towneley) و هنری پاور (Henry Power) کشف شده بود. او علاقۀ وافری به خصوصیات گازها داشت و موفق شد از طریق اعمال فشارهای مختلف روی یک سیلندر هوا (و با استفاده از جیوه برای سنجش میزان فشار) این حقیقت را اثبات نماید که در دمای ثابت، حجم گاز با فشار آن نسبت عکس دارد. به عبارت دیگر، حاصلضرب فشار در حجم گاز، مقداری ثابت است.
هر چند قانون بویل بیانی ریاضیوار از یک حقیقت طبیعی است، با این حال، اگر تغییرات چشمگیرتری روی فشار اعمال شود؛ قانون بویل کارایی لازم را نخواهد داشت و باید کمی دستکاری شود. این مطلب ۲۰۰ سال پس از انتشار قانون بویل کشف شد. قانون گاز ایده آل نسخۀ جامعتری از قانون بویل میباشد. در مقالات بعد به نسخۀ بهروزتر قانون بویل خواهیم پرداخت.