تکنیک ARMS PCR (Amplification Refractory Mutation System) روشی استاندارد، آسان، سریع و قابل اتکا برای تشخیص جهشهای نقطهای و پلیمورفیسمها و یا حذفهای کوچک است. این روش برای افتراق اللهای یک ژن که تفاوت آنها به کوچکی یک جفتباز است به کار میرود. ARMS PCR نخستین بار در سال ۱۹۸۹ توسط Newton و همکارانش و با بررسی نقصهای ژن α۱-antitrypsin معرفی شد و به Allele specific PCR نیز معروف میباشد. این تکنیک همچنین میتواند افراد هتروزیگوت و هوموزیگوت از لحاظ یک لوکوس ژنی را از همدیگر افتراق دهد. ARMS PCR برخلاف سایر تکنیکهایی که برای تشخیص اللها استفاده میشوند، نیازی به استفاده از آنزیمهای محدودکننده و آنالیز توالی محصولات PCR ندارد.
طراحی یک ARMS PCR دقیق و قابل اتکا نیازمند تعیین ترکیبی مناسب از توالی پرایمر و شرایط واکنش است تا درنهایت از الل هدف، محصولی قابل شناسایی تولید شود و اتصال پرایمر ARMS به توالیهای غیراختصاصی به حداقل برسد. راهحل این مسئله استانداردسازی متغیرها تا بیشترین حد ممکن است. از جمله این متغیرها میتوان به پارامترهای چرخه حرارتی، غلظت آنزیمها و توالی و غلظت پرایمر ARMS اشاره کرد.
در طی سالهای گذشته تعداد قابل توجهی از ژنها توالییابی شده و نیز جهشهای و پلیمورفیسمهای فراوانی که از لحاظ بالینی نیز مهم هستند، شناخته شدهاند. در نتیجه امروزه نیاز فراوانی به بررسی واریانتهای ژنوم انسان در زمینه بیماریهای ارثی، تشخیص سرطان، tissue typing در پیوند عضو و تعیین استعداد ابتلا به بیماریها احساس میشود. تکنیک مورداستفاده برای چنین آنالیزهایی باید ساده و قابل اتکا بوده و امکان بررسی چندین جهش به صورت همزمان را فراهم آورد و نیز برای تمام جهشهای نقطهای قابل استفاده باشد. تکنیک ARMS این خصوصیات را داراست و میتواند به صورت روتین به این منظور مورد استفاده قرار گیرد.
مقاله مرتبط: PCR چیست؟
پرایمرهای ARMS
تکنیک ARMS پرایمرهایی را به کار میگیرد که برای توالی موردنظر اختصاصی هستند. این پرایمرها تنها زمانی به آن توالی اجازه تکثیر میدهند که الل هدف در نمونه موجود باشد و سایر اللها تکثیر نخواهند شد. پس از انجام واکنش ARMS حضور محصولات PCR و یا عدم حضور آنها مشخصکننده حضور و یا عدم حضور الل هدف است.
اساس طراحی پرایمر در ARMS PCR بر این مشاهده استوار است که در شرایط مناسب، الیگونوکلئوتیدهایی که در انتهای ۳’ مکمل توالی هدف نیستند، نمیتوانند به طور مناسب به توالی هدف متصل شده و به عنوان پرایمر عمل کنند و درنتیجه واکنش تکثیر ادامه نمییابد. Mismatchهایی که بیشترین تاثیر را دارند عبارتند از: A:G، G:A و C:C. تاثیر سایر mismatchها متفاوت است.
علت این پدیده نبود خاصیت تصحیح اگزونوکلئازی ۳’ به ۵’ در Taq DNA پلیمراز است. در نتیجه باقی ماندن mismatch بین پرایمر و DNA الگو به شدت بازده فرایند تکثیر را کاهش میدهد. DNA پلیمرازهای high fidelity که دارای این خاصیت هستند نمیتوانند در ARMS به کار گرفته شوند. از جمله این DNA پلیمرازها میتوان به Vent و Pfu اشاره کرد.
پرایمر ARMS به صورتی طراحی میشود که نوکلئوتید ۳’ انتهایی آن اختصاصی الل هدف باشد. در نتیجه این پرایمرها میتوانند به دو صورت طراحی شوند: پرایمر نرمال (N) که انتهای ۳’ آن مکمل الل طبیعی است و پرایمر جهشیافته (M) که انتهای ۳’ آن مکمل نوکلئوتید جهشیافته در الل مربوطه است. به عنوان مثال، اگر جهش جایگزینی از نوع A-T رخ داده باشد، نوکلئوتید آخر پرایمر الل جهشیافته، باید مکمل T، یعنی A باشد. پرایمر الل نرمال نیز در همان نقطه باید مکمل A، یعنی T باشد.
گاهی اوقات حتی در صورت مکمل نبودن انتهای ۳’ باز هم اتصال پرایمر رخ داده و توالی موردنظر تکثیر میشود. افزودن یک mismatch دیگر به موقعیتی در نزدیکی انتهای ۳’ میتواند این مشکل را حل کند و اختصاصیت واکنش را افزایش دهد. محدوده مکانی این mismatch در ۵ نوکلئوتید آخر پرایمر است اما معمولا واقع در باز ماقبل آخر قرار میباشد. انواع مختلف mismatchها خاصیت ناپایدارکنندگی متفاوتی دارند و برای انتخاب نوع آنها باید باز انتهایی را نیز در نظر گرفت. در صورتیکه mismatch ناشی از جهش، قوی و بسیار ناپایدارکننده باشد، mismatch باز ماقبل آخر باید از نوع ضعیف باشد و برعکس. توالی بقیه رشته پرایمر ARMS مکمل توالی هدف است.
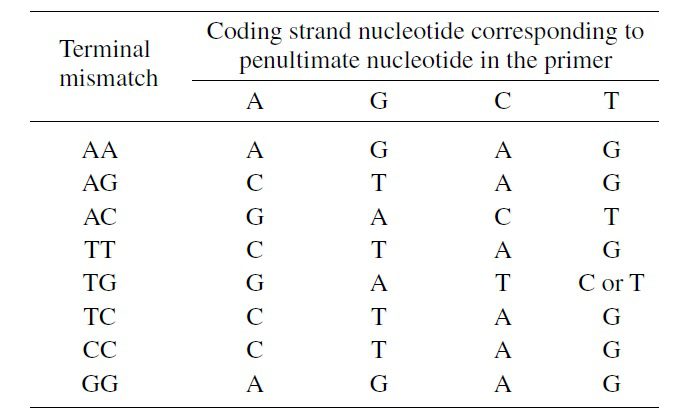
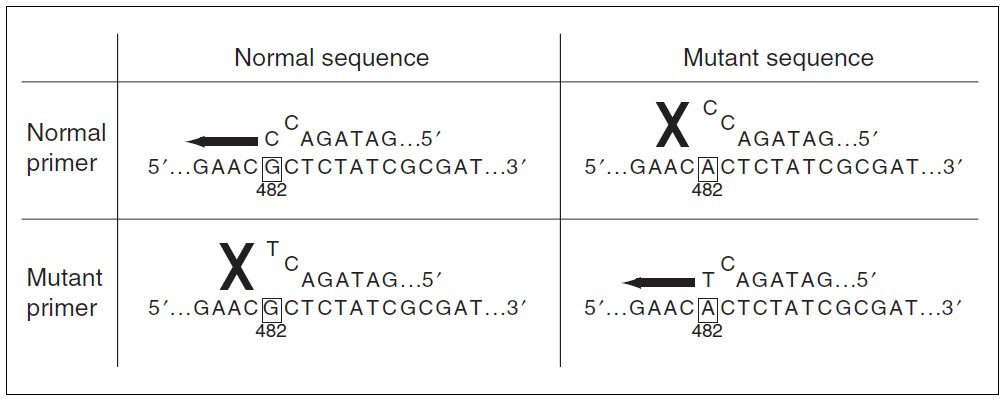
علت نامگذاری این تکنیک به ARMS آن است که پرایمر عادی در DNA الگوی جهشیافته و پرایمر اختصاصی الل جهشیافته نیز در DNA الگوی نرمال به PCR مقاوم (Refractory) است. درنتیجه یک پرایمر ARMS میتواند به گونهای طراحی شود که بتواند اللی خاص از یک سیستم چنداللی را تکثیر کند؛ درحالیکه نمیتواند عمل تکثیر الل دیگری را که تفاوت آن با الل هدف به کوچکی یک جفتباز است، انجام دهد.
الیگونوکلئوتیدی که به عنوان پرایمر ARMS استفاده میشود، باید طولی در حدود ۳۰ باز داشته باشد. پرایمرهای با طول کمتر از ۲۸ باز نباید مورد استفاده قرار گیرند. اما انواع بلندتر ممکن است استفاده شوند.
ARMS PCR استاندارد، Multiplex ARMS و Double ARMS از انواع این تکنیک هستند.
ARMS PCR استاندارد:
تکنیک ARMS PCR استاندارد به منظور بررسی یک جهش نقطهای منفرد به کار میرود. این تکنیک از دو واکنش مکمل تشکیل شده است که در دو لوله جداگانه انجام میگیرند. هر دو این واکنشها از یک نوع نمونه DNA استفاده میکنند. واکنش نخست حاوی پرایمر ARMSی است که اختصاصی DNA نرمال میباشد و نمیتواند DNA جهشیافته را در لوکوس ژنی موردنظر تکثیر کند. به طور مشابهی واکنش دوم دارای پرایمر ARMS مخصوص الل جهشیافته است و نمیتواند DNA نرمال را تکثیر کند.
پس پرایمرهایی که مورد استفاده قرار میگیرند سه نوع هستند. دو نوع اول پرایمرهای ARMS هستند که در انتهای ۳’ خود با همدیگر متفاوت میباشند و یکی از آن ها اختصاصی توالی DNA طبیعی و دیگری مخصوص توالی جهشیافته است. تنها یکی از این دو نوع در هر لوله آزمایش استفاده میشوند.
پرایمر سوم ثابت است و توالی مکملش در هر دو واکنش موجود است. این پرایمرها مخصوص نواحیای از ژن طراحی میشوند که معمولا فاقد جهش هستند و به عنوان کنترل داخلی به کار میروند. تکثیر ناحیه کنترل داخلی و عدم تکثیر ناحیه متصل به پرایمر ARMS نشاندهنده نتیجه منفی حقیقی است. اما در شرایط منفی کاذب، نه کنترل داخلی و نه پرایمر ARMS تکثیر میشود.از جمله عوامل حصول نتیجه منفی کاذب عبارتند از: مقادیر خیلی زیاد یا خیلی کم DNA، کیفیت پایین DNA الگو، اضافه نشدن پرایمر، Taq و یا سایر مواد اولیه و وجود مواد مهارکننده PCR.
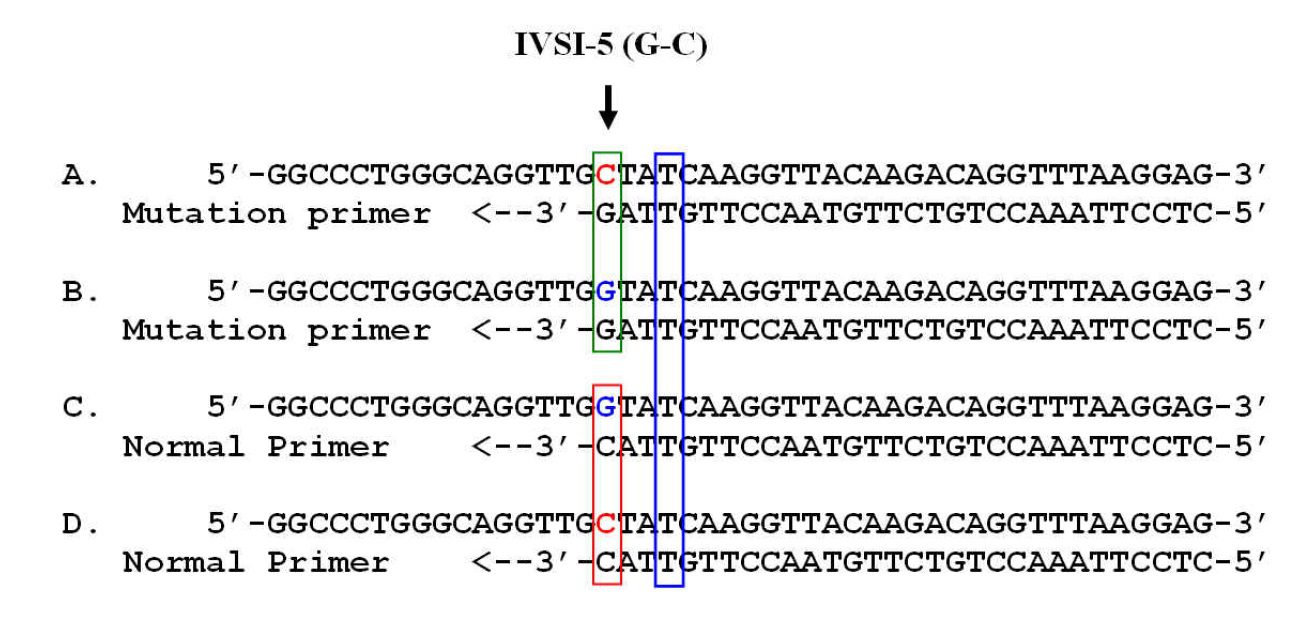
روش کلی انجام فرایند به این صورت است که ابتدا پرایمرهای ARMS نرمال و جهشیافته و پرایمرهای کنترل مناسب طراحی میشوند. سپس مخلوط اولیه واکنشهای جهشیافته و نرمال تهیه و در لولههای مناسب استفاده در Thermal cycler جای میگیرد. در مرحله بعدی DNA کنترل و نیز کنترلهای داخلی (در صورتیکه جزو ساختار DNA الگو نباشند؟؟؟) افزوده میشوند. پس از اضافه کردن Taq DNA پلیمراز، لولههای آزمایش در Thermal cycler قرار میگیرند. استفاده از Hot start PCR باعث میشود که اتصال غیراختصاصی پرایمر به توالی الگو رخ ندهد. در نهایت محصولات واکنش الکتروفورز و آنالیز میشوند.
پس از الکتروفورز هر ستون از لحاظ سایز باندهای تشکیل شده برای قطعات کنترل و ARMS بررسی میشود. برای هر دو نوع واکنش ARMS نرمال و جهشیافته سه حالت را میتوان متصور شد:
- نتایج موردانتظار: اگر الل هدف در نمونه موجود باشد، محصول ARMS ظاهر میشود و در غیر این صورت محصولی مشاهده نخواهد شد. در صورتیکه ژنوتیپ نمونه هوموزیگوس جهشیافته و یا هوموزیگوس طبیعی باشد، واکنش تکثیر تنها در یکی از لولهها رخ خواهد داد. در صورتیکه نمونه هتروزیگوس باشد تکثیر در هر دو لوله انجام خواهد شد.
- نتیجه غیراختصاصی: هم در صورت وجود الل و هم در صورت نبود آن، محصول ARMS همچنان مشاهده میگردد. برای افزایش اختصاصیت واکنش در این حالت میتوان واکنش را تکرار و این بار میزان پرایمرهای ARMS را در هر دو مخلوط واکنش کاهش داد. در صورتیکه این حالت مجددا مشاهده میتوان از mismatchهای قویتری در باز ماقبل آخر استفاده کرد.
- نتیجه intensive: هم در صورت وجود توالی هدف و هم در صورت نبود آن هیچ محصولی مشاهده نمیشود. به منظور بهینهسازی این حالت میتوان میزان پرایمرهای ARMS را در هر دو مخلوط واکنش افزایش و یا غلظت پرایمرهای کنترل را کاهش داد. اگر همچنان محصولی مشاهده نشد، باید قدرت mismatch موجود در باز ماقبل آخر را کاهش داد.
به این ترتیب میتوان حساسیت و اختصاصیت واکنش ARMS را با تغییر شرایط واکنش از جمله توالی پرایمر و یا غلظت آن تنظیم کرد. باید در نظر داشت که تغییر mismatch باز ماقبل آخر در پرایمر حساسیت و اختصاصیت واکنش ARMS را به میزان زیادی دگرگون میکند. این در حالی است که تغییر غلظت پرایمر تغییرات زیادی در این مورد ایجاد نمیکند و برای تنظیم واکنش مناسبتر است. همچنین طراحی پرایمر مناسب، دمای اتصال (annealing) بالا و تعداد محدود چرخهها میتواند از نتایج کاذب جلوگیری کند.
مهمترین مزیت ARMS PCR این است که مراحل تکثیر قطعات مربوط به الل موردنظر و تشخیص آنها با یکدیگر ترکیب شدهاند. در این حالت حضور محصول موید حضور الل موردنظر است و برعکس. این موضوع باعث صرفهجویی در زمان میشود، اما دقت واکنش را نسبت به سایر واکنشهایی که در آنها این دو مرحله تفکیک نشدهاند کاهش میدهد. در چنین واکنشهایی به دنبال PCR، از آنزیم محدودکننده برای بررسی قطعات استفاده میشود.
تکنیک Multiplex ARMS PCR
در بررسی جهشهای نقطهای موجود در یک ژن، غالبا نیاز به بررسی آن ژن از لحاظ وجود یا عدم وجود چندین جهش داریم. از راههای انجام این بررسی، اجرای چندین آزمایش ARMS منفرد و یا یک آزمایش Multiplex ARMS PCR است. Multiplex ARMS، استفاده از تکنیک ARMS را به منظور تعیین ژنوتیپ سیستمهای چند اللی تسهیل میکند. در Multiplex ARMS چندین پرایمر ARMS اختصاصی الل هدف به یک لوله آزمایش افزوده میشوند و تنها یک واکنش انجام میگیرد. اساس این روش مشابه تست ARMS استاندارد است؛ با این تفاوت که چندین پرایمر در یک ظرف واکنش حضور دارند و بهینهسازی توالی و غلظت همه آنها در ارتباط با هم بر پیچیدگی واکنش میافزاید.
مقاله مرتبط: تکنیک Multiplex PCR
در نهایت محصولات توالیهای مختلف از روی مشخصات فیزیکی مانند اندازه از همدیگر افتراق داده میشوند. در نتیجه بهتر است واکنش را به گونهای طراحی کرد که تفاوت سایز محصولات PCR بزرگتر از ۵۰ جفتباز باشد. همچنین در تکنیک multiplex ARMS نباید از مقادیر بالای mismatchهای ناپایدارکننده استفاده نمود.
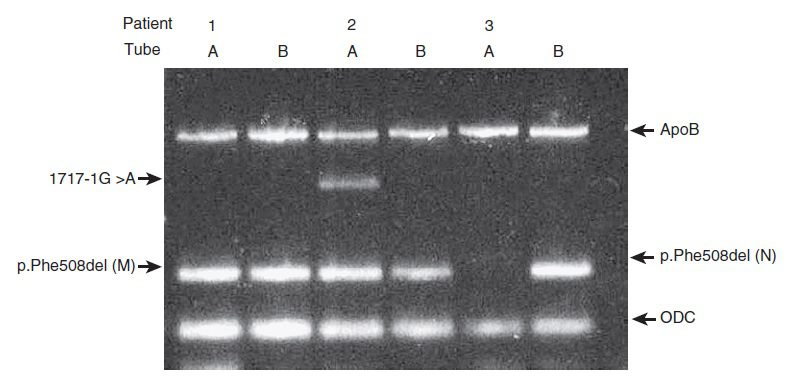
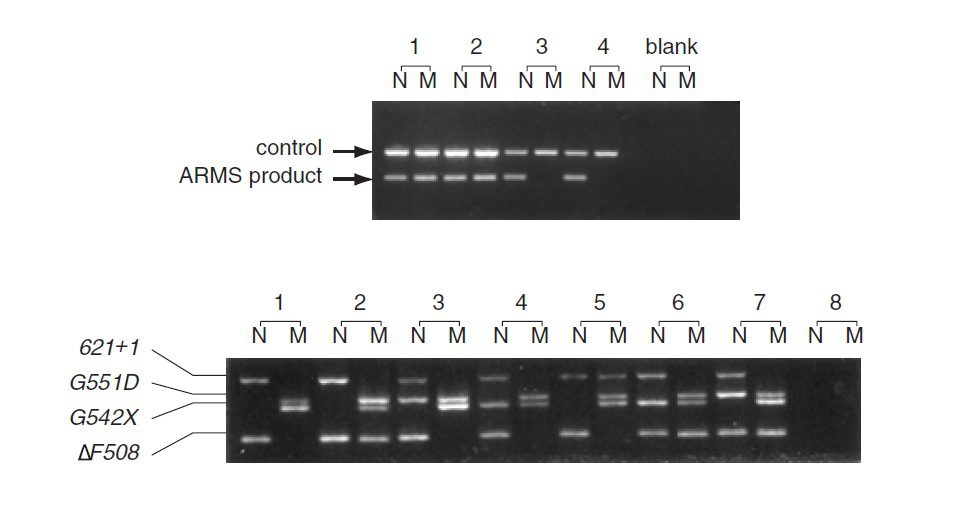
تست ARMS استاندارد و Multiplex ARMS؛ پنل بالایی نشاندهنده نتایج تست جهش R117H موجود در ژن CFTR است که بر روی ۴ نفر انجام گرفته است. هر تست ARMS متشکل از دو واکنش است که هر کدام اختصاصی الل نرمال و جهشیافته هستند. همه ستونها حاوی محصول کنترل PCR هستند که طولی به اندازه ۳۶۰bp دارد. نمونههای ۱ و ۲ مربوط به افرادی هتروزیگوت از لحاظ جهش R117H میباشند. افراد ۳ و ۴ نرمال هستند. پنل پایینی نتیجه تست ۴ جهش معمول ژن CFTR را که بر روی ۷ نفر صورت گرفته است، نشان میدهد. این جهشها عبارتند از: ΔF508، G542X، G551D و ۶۲۱+۱ G→T. برای هر نمونه دو ستون وجود دارد. ستون نخست حاوی باندهای مربوط به محصولات پرایمر ARMS نرمال برای ۶۲۱+۱ G→T و ΔF508 و محصولات پرایمر جهشیافته برای G551D و G542X است. ستون دوم دقیقا عکس ستون اول میباشد. ژنوتیپهای مربوط به این هفت نمونه عبارتند از: ۱، نرمال؛ ۲، هتروزیگوت برای ΔF508؛ ۳، هتروزیگوت برای G551D؛ ۴، هتروزیگوت برای G542X؛ ۵، هتروزیگوت برای ۶۲۱+۱G→T؛ ۶، هتروزیگوت برای G542X و ΔF508؛ ۷، هتروزیگوت برای G551D و ΔF508.
تکنیک Double ARMS
در این تکنیک دو پرایمر اختصاصی الل موردنظر به طور همزمان در یک واکنش استفاده میشوند. تکثیر تنها زمانی رخ میدهد که اللهای اختصاصی پرایمرهای ARMS مورد استفاده بر روی یک کروموزوم واقع باشند. به این ترتیب تکنیک Double ARMS PCR روشی قدرتمند برای تعیین ارتباط نواحی پلیمورفیک است. به عبارت دیگر این تکنیک مشخصکننده هاپلوتایپها است.
Double ARMS در بررسی هاپلوتایپها از متدهای دیگر موثرتر است. همچنین این تکنیک در تعیین ژنوتیپ سیستمهای چنداللی که در آنها افتراق هر الل از سایر اللها توسط وجود ترکیب متفاوتی از نواحی پلیمورفیک انجام میگیرد، موثر است. HLA-typing از جمله مهمترین مثالهای این کاربرد است.
تکنیک Double ARMS همچنین دارای اختصاصیت بیشتری در مقایسه با ARMS استاندارد است. درنتیجه میتوان به وسیله آن میزان اندکی از DNA موردنظر را که در پسزمینهای از سایر مولکولهای DNA فراوانتر قرار دارد، تشخیص داد. تشخیص سلولهای جنینی در خون مادر وتشخیص کایمریسم پس از پیوند مغز استخوان از جمله کاربردهای این مزیت است.

عالی هستید