تغییر دادن برنامهی ژنتیکی یک فرد، آسانتر از چیزی است که شاید فکرش را بکنید. در حالی که تکنیکهای تغییردهندهی DNA در سطح مولکولی در حال گسترش اند، امکان خاموش و روشن کردن آنها بدون ایجاد تغییر دائمی در مادهی ژنتیک نیز وجود دارد. این یعنی ما میتوانیم دستورالعملهای ژنتیکی را که به بدن یک ارگانیسم فرستاده میشود، با تغییر در محیط آن یا داروها دستکاری کنیم.
این زمینهی تحقیقاتی در مبحث “اپیژنتیک” در حال حاضر به پزشکان کمک میکند تا مکانیسم برخی از بیماریها را درک کنند. این که چرا ورزش کردن میتواند مفید واقع شود، و یا چگونه میتوانیم پروسهی پیری را تغییر دهیم، نیز جزو این زمینه از تحقیقات اند. در این میان، برخی نیز به دنبال بررسی نقش اپیژنتیک در باکتریها هستند.
اخیراً راهی بالقوه برای تغییرات اپیژنتیک در باکتریها که شاید ما را از آنتیبیوتیکها بینیاز کند، مورد توجه قرار گرفته است. این تلاشها، با در نظر گرفتن روند رو به رشد مقاومت آنتیبیوتیکی بسیار حائز اهمیت است.
این مطالعات روی باکتری Acinetobacter baumannii انجام شده است. این گونهی باکتریایی یکی از دلایل عمدهی عفونتهای بیمارستانی است و نرخ مرگومیر آن به ۷۰ درصد نیز میرسد. در حال حاضر برخی از سویههای A. baumannii به حدی مقاوم شدهاند که سازمان بهداشت جهانی آنها را در صدر فهرست بزرگترین تهدیدهای باکتریایی برای سلامت انسان قرار داده است.
محققان داروهایی با عنوان “داروهای آنتیویرولانس” معرفی کردهاند که به جای کشتن باکتریها، آنها را بیخطر میسازد. در این شرایط به سیستم ایمنی بدن اجازه داده میشود تا باکتریها را از بدن پاکسازی نماید؛ همچنین با پدیدهی مقاومت آنتیبیوتیکی هم دیگری کاری نخواهیم داشت. یافتن راهی برای اثر گذاشتن بر اپیژنتیک باکتریها، سویههای مقاوم آنها را بیخطر کرده و به تولید داروهای آنتیویرولانس جدید منجر خواهد شد.
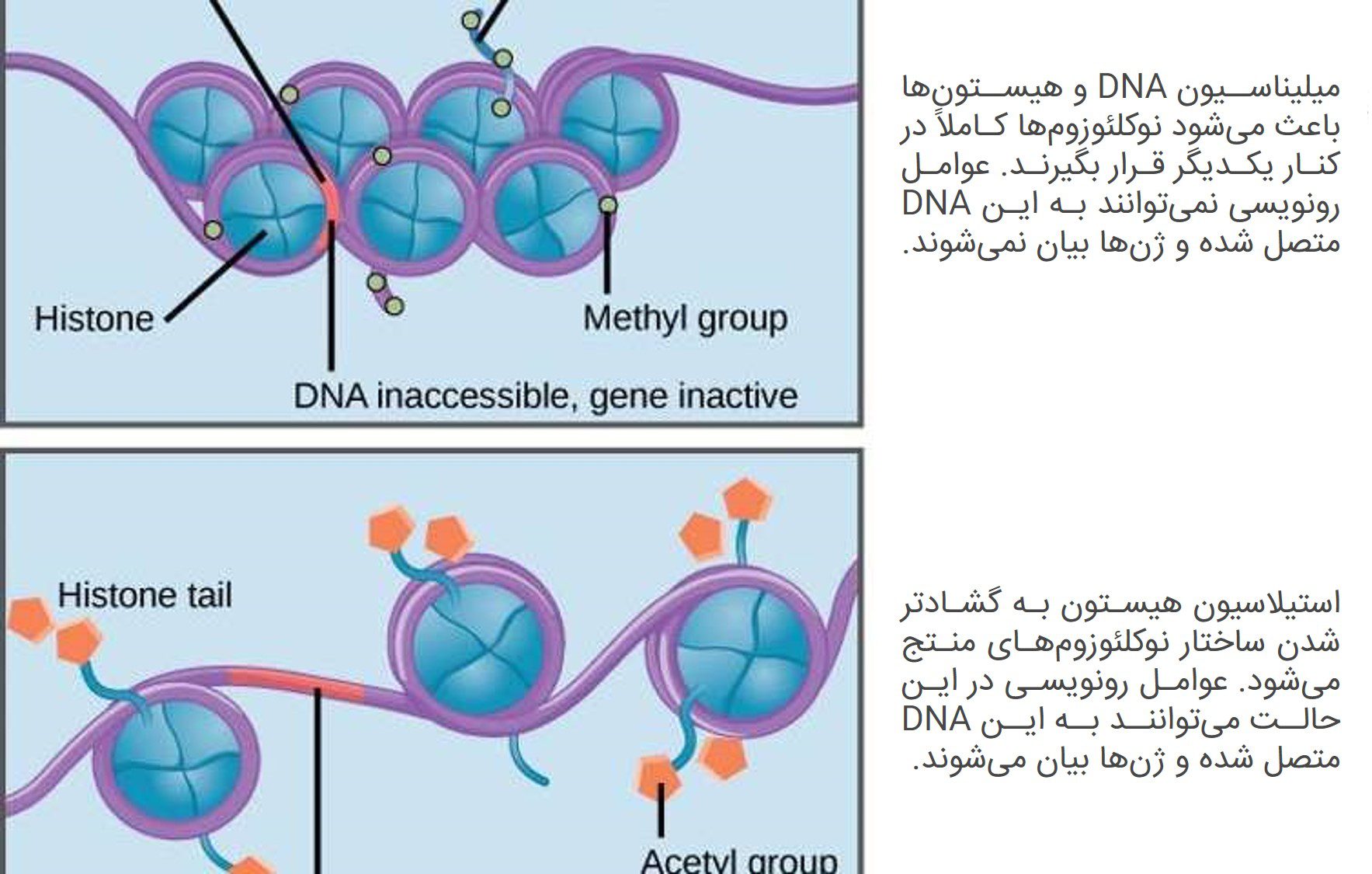
برای آغاز این فرآیند، ابتدا از اپیژنتیک انسانی شروع میکنیم. معمولترین راه برای اثرگذاری روی اپیژنتیک ما اضافه کردن ضمائم مولکولی کوچک (tag) به مادهی ژنتیک میباشد که تنظیم بیان ژن را تحت تأثیر قرار میدهد. میتوان تَگی مثل گروه استیل را به پروتئین مهمی مثل هیستون متصل کرد.
هیستونها مولکولیهای DNA دو متری ما را سازماندهی کرده و در فضایی به طول ۱۰۰ میکرومتر جا میدهند. اضافه کردن تگ استیل مکانیسم طبیعی سلولها برای تغییر برهمکنش هیستونها با DNA است. اضافه کردن تگ استیل، معمولاً برخی ژنها را فعال کرده و با این طریق به نوعی رفتارهای سلول را تغییر میدهد. عدم توانایی سلول در این پروسه، با انواع سرطانها، بیماریهای قلبیعروقی و بسیاری از اختلالات نورودژنراتیو ارتباط دارد.
سلولهای باکتریایی هم هیستونهای خودشان را دارند؛ این پروتئینها HU نام داشته و در سازماندهی DNA باکتریایی و عملکرد صحیح آن مؤثرند. باکتریهای گرم مثبت، مثل آنهایی که در سیستم گوارشی ما وجود دارند، بدون HUها قادر نیستند بقای خودشان راحفظ نمایند. باکتریهای گرم منفی (بیشترین عوامل عفونی انسان مثل سالمونلا انتریکا) نیز بدون HUها تا حد زیادی قدرت بیماریزایی خود را از دست میدهند.
داروهای جدید
با توضیحاتی که داده شد، اکنون نوبت میرسد به کاری که دانشمندان انجام دادهاند. اضافه کردن یک تگ استیل به HU، به صورت معناداری برهمکنش آن را با DNA تحت تأثیر قرار میدهد. این به آن معناست که چنین تغییراتی که روی اپیژنتیک تأثیر بگذارد، با احتمال بالا میتواند روی رشد و عفونتزایی ارگانیسمها مؤثر باشد. بنابراین اگر راهی به این شکل برای ایجاد تغییر در پروتئینهای باکتریایی وجود داشته باشد، یعنی شیوهی جدید برای توقف عفونتها یافتهایم.
این موضوع، چالش بسیار مهمی در پزشکی امروز است؛ چون باکتریهای مقاوم به آنتیبیوتیکها، سالانه ۷۰۰,۰۰۰ نفر را در سراسر جهان به کام مرگ میبرند. اگر درمانهای جدیدی پیدا نشود، این آمار قابلیت افزایش تا ۱۰ میلیون نفر در سال، تا ۲۰۲۵ را دارد.
اگر ارتباط بین تغییرات ویژهی اپیژنتیک و عملکرد باکتریایی را به خوبی مورد راستیآزمایی قرار دهیم، میتوانیم جستجوی موادی که بتوانند این تغییرات را اعمال نمایند، شروع کنیم. هماکنون چندین مولکول وجود دارد که با شیوهای بخصوص روی اپیژنتیک انسان تأثیر میگذارد؛ البته این مولکولها در مراحل پیشبالینی و کارآزماییهای بالینی قرار دارند. بنابراین دارویی که بتواند توان عفونتزایی باکتریها را خاموش کند، زیاد دور از تصور نیست.