رشد مجدد یک اندام از دست رفته، رویای بزرگی نیست. ستارهی دریایی و یا سمندر، جزو موجودات شناخته شدهای هستند که از این قابلیت استفاده کرده و بازو و دم جدید برای خود میسازند. این موجودات، ارگانهای ساخته شده را جایگزین ارگانهای از دست رفته میکنند. اما آنها تنها موجوداتی نیستند که از این قابلیت برخوردار هستند. شاخهای آهوی کوهی میتوانند دوباره جوانه زده و شاخههای فرعی تولید کنند. لازم به ذکر است که میزان این رشد تا بیش از ۳۰ کیلوگرم در عرض سه ماه نیز گزارش شده است. ماهیهای قزل آلا میتوانند قلب خود را بازآفرینی کنند. درحالیکه کرمهای پهن نشان دادهاند که میتوانند سرشان را از اول به وجود آورند.
سلولها به صورت انفرادی، همزمان با اینکه از بین میروند، دائما نیز جایگزین میشوند. این فرآیند جایگزینی بر اثر عواملی میتواند، کندتر شود. ولی باید این را دانست که این فرآیند، در طول زندگی فرد ادامه خواهد داشت. شما حتی میتوانید این بازآفرینی را به صورت ممتد در پوست خود مشاهده کنید. در حقیقت در انسان، هر دو الی چهار هفته به صورت کامل لایه خارجی پوست افتاده و به جای آن پوست تازه ساخته میشود؛ به عبارت دیگر بر اساس گفته جامعه شیمیدانان آمریکا، حدود ۵۱۰ گرم سلولهای پوستی در سال میشود.
به هر حال بازآفرینی کامل اندامها و قسمتهای بدن که عادت داشتیم در برنامههایی مثل “Doctor Who’s” شاهد آن باشیم، فراتر از محدودهی زیستشناسی انسان است. (Doctor Who’s برنامهی تلویزیونی بریتانیایی علمی-تخیلی است که از سال ۱۹۶۳ توسط BBC تولید میشود) اما در سالهای اخیر محققان به صورت موفقیت آمیز طیفی از ساختارهای بدن انسان را کشت دادند که ساختاری مشابه ساختار اصلی داشته و جواب آزمایش آنها بر روی حیوانات نیز موفقیت آمیز بوده است. ساختارهای کشت شده مقیاس کوچکتری از ارگانهای واقعی هستند و برای مطالعه عملکرد آنها و ساختار ارگان در حد جزئیاتی که قبلا قابل مطالعه نبود، به کار میروند. این ساختارها با نام ارگانوئید شناخته میشوند.
در اینجا به چند مورد از این ارگانوئیدها اشاره میکنیم:
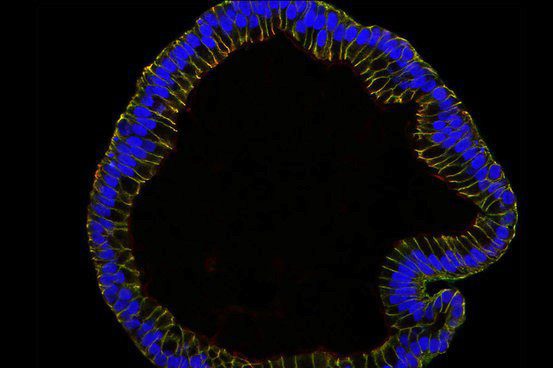
لوله فالوپ
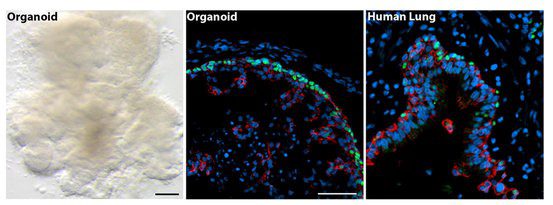
با استفاده از سلولهای بنیادی، محققانی از موسسه Max Planck که در مورد زیستشناسی عفونی در شهر برلین فعالیت میکنند، موفق شدند، لوله فالوپ را رشد دهند که بیشترین تعداد لایه سلولی را در بدن انسان دارد. این ساختار از یک طرف به تخمدان و از سمت دیگر به رحم وصل میشود. در گزارشی که در ۱۱ ژانویه سال گذشته منتشر شد، محققان در مورد ارگانوئید کشت داده شده توضیحاتی ارائه کردند که نشان میداد، ویژگی و مشخصات و شکل آن مانند لوله فالوپ در اندازه واقعی میباشد.
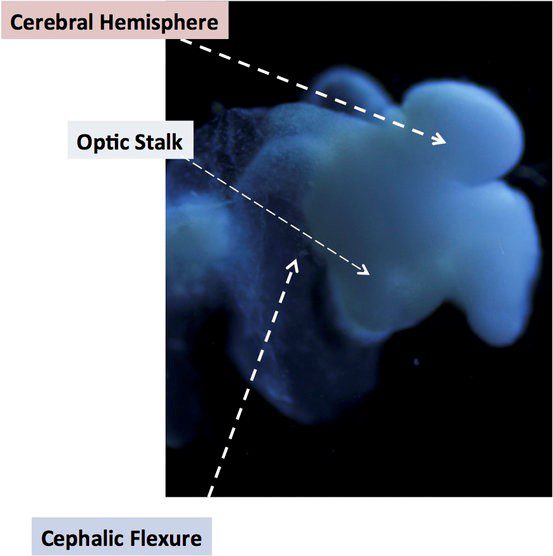
مغز کوچک
مغز رشد داده شده در آزمایشگاه که به اندازه پاککن سر مداد است، توسط محققان دانشگاه ایالت اوهایو (OSU) از سلولهای پوستی کشت داده شده است. این ساختار از لحاظ شکل و ژنتیکی مانند مغز جنین انسان ۵ هفتگی است. این مغز کوچک کشت داده شده که از آن به عنوان تغییر دهنده مغز توصیف میشود، اخبارش توسط OSU در ۱۸ آگوست طی گزارشی منتشر شد. این ارگانوئید که عملکرد نورونهای آن از طریق حمل پیامهای تحریکی مانند آکسون و دندریت صورت میگیرد. در شکلی که بالا آورده شده است، ساختارهای نشاندار شده معمولاً در مغز جنینی یافت میشوند.
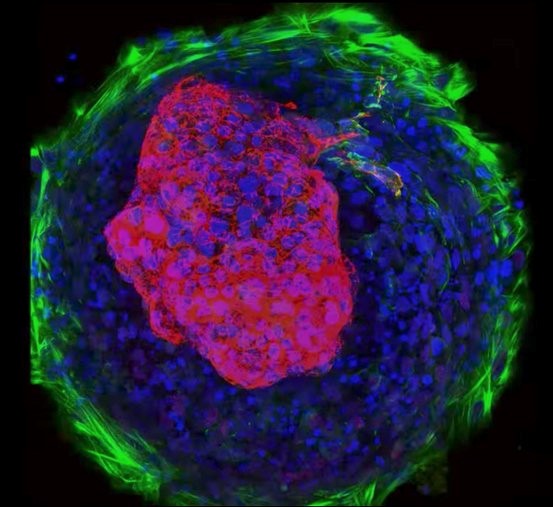
قلب کوچک
محققان با ارتقا سلولهای بنیادی میتوانند آنها را به بافت پیوندی و ماهیچه قلب تبدیل کنند. بعد از این عمل، با سازماندهی سلولها، اتاقکها و ضربان به وجود میآیند. در ویدیوئی که از این اقدام گرفته شده، سلولهای ماهیچهای قلب (با رنگ قرمز در وسط مشخص هستند) زمانی که توسط بافت پیوندی (حلقه سبز رنگ در اطراف) از اطراف تحت محافظت قرار میگیرند، شروع به ضربانسازی میکنند. Kevin Healy پروفسور مهندسی زیستشناسی و دبیر ارشد این مطالعه در گزارشی گفت:
این فناوری میتواند به ما کمک کند که به طور سریع تأثیر داروها بر قلب، مانند احتمال به وجود آمدن نواقص قلبی مادرزادی را مشاهده کنیم. همچنین از آن برای تشخیص این که کدام داروها در زمان بارداری و یا زمانهای دیگر، میتوانند خطرناک باشند، استفاده کرد.
این تحقیق در ۱۵ مارس سال ۲۰۱۵ در مجله nature communications چاپ شد.
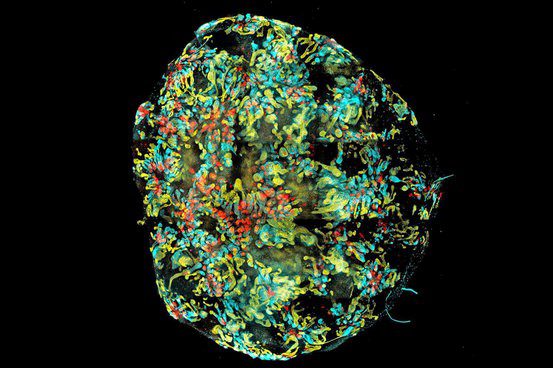
کلیه کوچک
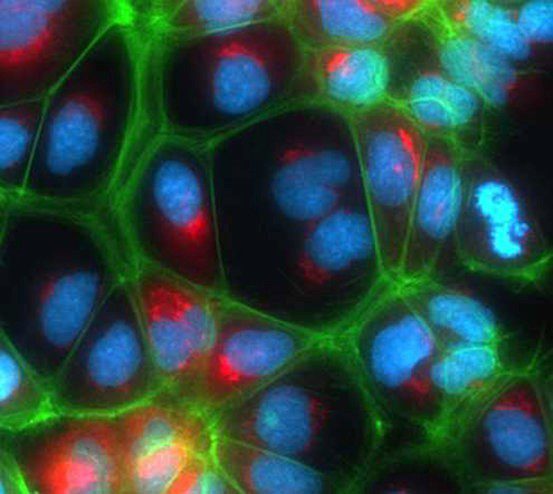
تیمی از دانشمندان استرالیایی از تغییر دادن سلولهای بنیادی، کلیه کوچکی را برای اولین بار پرورش دادند. فرآیند رشد این کلیه، زیر نظر محققان و کاملاً مطابق با رشد کلیه طبیعی بود. این کلیه، شامل سه نوع سلول میشود. در عکس بالا، سه رنگ مختلف، انواع سلولهای کلیه که در طول زمان، نفرونها را خواند ساخت، نشان میدهد.
ریه کوچک
محققانی از موسسههای متعدد با همکاری هم، ارگانوئید ریه سه بعدی را کشت دادند. این ارگانوئید از برونشی، ساختارهای راههای هوایی و کیسههای ریوی ساخته میشود. Jason R. Spence سردبیر این تحقیق و استادیار پزشکی داخلی و سلولی دانشگاه میشیگان در مورد نتیجه تحقیقات طی گزارشی گفت:
این ارگانوئیدها میتوانند عملکردی مانند عملکرد بافت واقعی انجام دهند. به علاوه، مدل خوبی برای مطالعه چگونگی تشکیل ارگان و تغییرات آن در زمان بیماری و یا اینکه نسبت به یک داروی جدید، ریه چه واکنشی نشان میدهد، است.
لازم به ذکر است که ارگانوئید ریه پرورش داده شده، بیش از صد روز در آزمایشگاه زنده ماند.
معده کوچک
برای تشکیل ارگانوئید معده در ظرف مخصوص کشت حدود یک ماه وقت لازم است. بعد این مدت، معده به شکل تخم و ساختاری توخالی دیده میشود. Jim Wells دبیر ارشد این تحقیق و استاد زیستشناسی تکاملی در مرکز پزشکی کودکان شهر سینسیناتی درباره این تحقیقات به Live science گفت:
این معدههای عروسکی که اندازه هر کدام از آنها در حدود یک دهم اینچ (۳ میلیمتر) است؛ در بعضی تحقیقات مخصوصاً تحقیق در مورد عوامل باکتریایی خاص که باعث به وجود آمدن بیماریهای مربوط به معده میشود، بسیار مفید خواهد بود. این امر به این خاطر بهتر است که واکنش عوامل باکتریایی در معده حیوانات آزمایشگاهی با معده انسان متفاوت خواهد بود.
واژن
در آوریل ۲۰۱۴ مقالهای در مجله The Lancet منتشر شد که در مورد کاشت موفقیت آمیز واژنهای رشد داده شده در آزمایشگاه، در بدن انسان توضیح داده بود. این ارگانوئیدها با پرورش دادن سلولهای خود بیمار در چهارچوبی به شکل واژن به وجود میآیند. پیوند این ارگان از چندین سال قبل در دختران ۴ ساله و زنان جوان بین ۱۳ تا ۱۸ سال که به صورت مادرزادی واژن یا مجاری ادراری نداشتند و یا اینکه ارگان به طور کامل رشد نکرده بود، انجام میگرفت. این افراد به مدت ۸ سال بعد از پیوند، تحت نظر خواهند بود؛ یعنی تا زمانی که ارگان عملکرد نرمالی داشته و فرد بتواند مقاربت جنسی بدون درد داشته باشد.
آلت تناسلی
محققان در موسسه Wake Forest با استفاده از سلولهای خرگوش، بافتی را به وجود آورند که حالتی مانند بافت آلت قابل نعوظ داشت. بعد از این عمل، محققان با پیوند آن به خرگوش نر، کارکرد آن را مورد آزمایش قرار دادند. نتیجه این پیوند، موفقیت آمیز بود و خرگوش موفق به برقراری رابطه جنسی شد. با وجود این موفقیتها فعلاً این تحقیق در مرحله آزمایشگاهی بوده و برای گسترش کار و آزمایش بر روی انسان، نیازمند تایید از طرف سازمان غذا و دارو آمریکا است. موسسه بازآفرینی پزشکی ارتش آمریکا، یکی از حامیان مالی این برنامه میباشد. زیرا از طریق آن، میتوانند به سربازانی که در طول جنگ دچار آسیب از این ناحیه شدهاند، کمک کنند تا بهبود یابند.
مری
تیمی بینالمللی در دانشگاه پزشکی ایالت کوبان در کراسنودار روسیه، توانستند مری را از طریق رشد دادن سلولهای بنیادی در چهارچوبی به وجود آوردند که عملکرد نرمالی داشت. این کشت، حدود سه هفته طول کشید که بعد از آن به صورت موفقیتآمیز در موشها پیوند زده شد. دانشمندان، مریهای جدید را به جهت کنترل دوام آنها ۱۰ هزار دفعه با باد پر و خالی کردند. بعد از این آزمایش، این ساختارهای مصنوعی در ۱۰ موش پیوند زده شد که در ۲۰ درصد حیوانات توانست به جای ارگان اصلی، عملکرد قابل قبولی داشته باشد.
گوش
دانشمندان توانستند به صورت سه بعدی از گوش انسان پرینت بگیرند. آنها ابتدا قالبی از گوش یک بچه تهیه کردند. سپس آن را پرینت کرده و بعد از این کار، سطح قالب پرینت شده را با سلولهایی پوشاندند. و نهایتاً این سلولها در اطراف قالب شروع به رشد کردند. سپس دانشمندان به داخل قالب پوشیده از سلول، سلولهای گوش و کلاژن گاوی تزریق کردند. Live Science در این مورد گفت “یک گوش ظاهر شد”.
در مرحله آخر، محققان گوشهای ساخته شده را بر روی موشها به مدت یک الی سه ماه پیوند زدند. در طول آن محققان همانند ارگانی که رشد میکند، تغییرات سایز و شکل آن را تحت نظر داشتند.
مقاله مرتبط: ارگان-روی-چیپ؛ فناوری نوین چاپ سهبعدی
سلولهای کبدی
کبد بزرگ ترین اندام در داخل بدن انسان است که اگر در جای مناسب خود باشد تعمیر، ترمیم و بازیابی عالی خواهد داشت ولی بیرون از بدن با چالش روبهروست. به دفعات برای دانشمندان اثبات شده که نمیتوانند سلولهای کبدی یا هپاتوسیتها را پرورش داده و زنده نگه دارند. برای اولین بار، دانشمندان آلمانی و اسرائیلی توانستند با موفقیت، هپاتوسیتها را در آزمایشگاه زنده نگه دارند. نتایج این مطالعه در ژورنال Nature Biotechnology منتشر شد. با این که این سلولها را حتی ارگانوئید هم نمیشود نامید، ولی امیدها را برای مطالعات بالینی زنده میکند.




سلام
خواستم بدونم که برای ساخت خون انسان در لابراتور، چه رشته دانشگاهی رو باید دنبال کنم؟
ممنون از وقتی که میگذارید