تشخیص سرطان غالبا درمانهایی غیراختصاصی را به دنبال دارد. از جمله این درمانها رادیوتراپی، شیمی درمانی و جراحی است که علاوه بر تومور به سلولهای سالم بدن هم آسیب میزند. پژوهشگران به دنبال روشهایی هستند که تومورها را بدون ایجاد آسیبهای جانبی حذف کنند و در این میان روشهایی توسعه پیدا کردهاند که تومورهای خاصی را هدف قرار میدهند. اخیرا روشهایی نیز ایجاد شدهاست که سیستم ایمنی را طوری تنظیم میکند تا بتواند به نحو موثرتری با سرطان مبارزه کند. شواهد نشان دادهاند که چنین ایمونوتراپیهایی سیستم ایمنی بیمار را علیه مولکولهایی تحریک میکنند که باعث تفاوت سلولهای سرطانی از سلولهای عادی میشوند. در نتیجه سلولهای T به سمت هدف هجوم برده و آن را تخریب میکنند.
اساس این روش جهشهایی است که مرتب در سلولهای سرطانی رخ داده و منجر به تولید آنتی ژن هایی میشود که به طور گسترده در داخل و سطح سلولهای سرطانی بیان میشوند. با آمادهسازی سیستم ایمنی در جهت هدف قرار دادن آنتی ژنهای اختصاصی تومور، یا همان نئو آنتی ژن ها، پژوهشگران خواهند توانست به صورت انتخابی سلولهای سرطانی را بدون آسیب به سلولهای سالم خودی، نابود کنند.
مقاله مرتبط: درمان سرطان روز به روز شخصیتر میشود
سرطان: بیماری جهشها
سرطان معمولا از یک سلول شروع میشود. با تقسیم این سلول و تشکیل کلونی، جهشهای تغییردهنده عملکرد در ژنهای کنترل کننده رشد، بقا و تمایز سلولی تجمع مییابد. این مفهوم کلی تعیینکننده نحوه درک بیماری و درمان آن است. اتفاقی که حین تبدیل سلول نرمال به سلول نئوپلاستیک (سرطانی) رخ میدهد، تجمع جهشهایی است که عملکرد اساسی سلولها را تحت تاثیر قرار میدهند. یافتهای که پژوهشگران اخیرا به آن دست یافتهاند، این موضوع را تایید میکند: در مراحل اولیه ایجاد سرطان، جهشهای مکرری در عملکرد پروتئینهای ترمیم کننده DNA رخ میدهد و در نتیجه انباشته شدن جهشها در تومور تسهیل میشود.
میزان جهش در انواع مختلف تومور تفاوت فراوانی دارد. بافتهایی که بیشتر در معرض عوامل جهشزا قرار دارند مانند پوست، روده و مثانه، بیشترین میزان جهش در تومور را دارند. رتبه دوم از آن تومورهایی است که فاقد سیستمهای اصلاح همانندسازی مانند proofreading و DNA mismatch repair هستند؛ مانند زیرگروههای مشخصی از سرطانهای کولورکتال و اندومتر رحم. برخی از این جهشها انکوژن هستند و Driver نام دارند؛ این در حالی است که تعداد فراوانی از آنها نقش مشخصی در ایجاد و حفظ سرطان نداشته و جهشهای passenger نامیده میشوند.
مقاله مرتبط: میزان جهش در تومور: راهی برای پیشبینی پاسخ به درمان
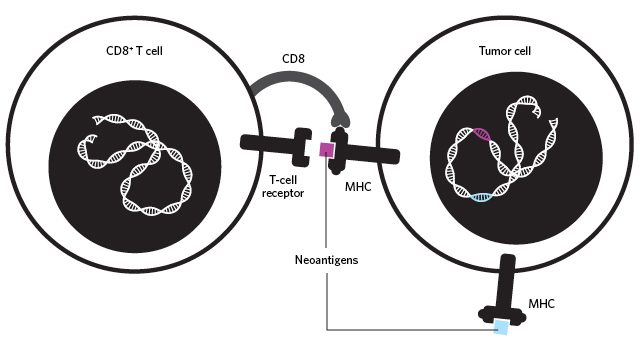
هر دو نوع جهش driver و passenger میتوانند آنتیژنهای اختصاصی تومور یا نئو آنتی ژن ها را ایجاد نمایند که توسط لنفوسیتهای T شناسایی میشوند. Tسلها معمولا پپتیدهای کوتاه و خطی مشتق از پروتئینهای داخل سلولی و خارج سلولی پاتوژنها را که بر روی مولکولهای MHC ارائه میشوند، تشخیص میدهند. MHCها در سطح تمام سلولهای بدن یافت میشوند و پپتیدهای سلولهای خودی که به آن متصل میشوند، طی فرایندی که tolerance نامیده میشود، غالبا نادیده گرفتهمیشوند. پپتیدهایی که در توالی حتی به اندازه یک آمینواسید با پپتیدهای خودی متفاوتند، توسط T سلها به نحو موثری هدف قرار داده میشوند.
حضور پپتیدهای بیگانه بر سطح سلولهای آلوده به باکتریها یا ویروسها، از مدتها پیش شناخته شده است. پژوهشگران اخیرا به ظهور مولکولهای بیگانه در سطح سلولهای توموری نیز پی بردهاند. این آنتیژنها میتوانند برای کنترل تومور بهکارگرفتهشوند. مطالعات حیوانی فراوانی وجود خاصیت آنتیژنیسیته را در تومورها نشان دادهاست؛ به این معنی که سیستم ایمنی خصوصا سلولهای CD4+ و CD8+ میتوانند از ایجاد دوباره همان نوع تومور جلوگیری کنند.
نوع دیگری از ایمونوتراپی که در آن نئو آنتی ژن های توموری نقش دارند، مهار کنندههای نقاط وارسی ایمنی (Immune Checkpoint Inhibitors) هستند. این نوع از درمان سیگنالهای بازدارنده Tسلها از مقابله با سرطان را مهار میکنند. در هر دو نوع مطالعه حیوانی و انسانی، استفاده از آنتیبادیها برای متوقف کردن مسیرهای وارسی ایمنی مانند PD-1/PD-L1 و CTLA-4 میتواند باعث آغاز پاسخهای ضدتوموری شدیدی از جانب Tسلها شود.
هر چه تعداد نئو آنتی ژن های سلولهای سرطانی بیشتر باشد، احتمال وجود رسپتوری که با یکی از این آنتی ژنها تطابق داشته باشد، بیشتر خواهد شد. همچنین مطالعات بالینی فراوانی که پیوند Tسلها را بررسی کردهاند، نشان دادهاند که محصولات ژنهای جهشیافته، اهداف لنفوسیتهای منتقل شده هستند. مطالعات فراوان انجام شده و نیز نتایج به دست آمده از تک تک بیماران دلایل قانعکنندهای برای هدف قرار دادن نئو آنتی ژن ها برای درمان سرطان فراهم میکند. قدم بعدی، تعیین مارکرهای اختصاصی برای هر نوع سرطان و آمادهسازی سیستم ایمنی به منظور هدف قرار دادن به طور موثرتر است.