آنتیبادیها یکی از مهمترین ابزارهای دفاعی بدن در برابر میکروبهای بیماریزا هستند. اما یکی از این پروتئینهای سیستم ایمنی، به یکی از باکتریهای غیر بیماریزا کمک میکند تا در رودهای انسان، ساکن شده و جزیی از میکروبیوم طبیعی و ثابت بدن شود.
ظاهرا این باکتری سطح خودش را با ایمونوگلوبولین A پوشانده و به مخاط موکوسی پوشانندهی روده وصل میشود. با این اتصال، باکتری در روده باقی مانده و جزء جداییناپذیری از میکروبیوم طبیعی روده را تشکیل میدهد.
IgA یکی از فراوانترین ایمونوگلوبولینهایی است که در بدن پستانداران تولید میشود. این یافته در موشهای ایزوله (بدون میکروب) بدست آمده و احتمالا روزی به محققان کمک خواهد کرد تا برای درمان بیماریهای مختلف، میکروبهای خاصی را به بدن انسان اضافه کنند.
دکتر Sidonia Fagarasan، ایمونولوژیستی از موسسهی RIKEN Yokohama در ژاپن، اعلام میکند اتفاقاتی که بین باکتریها و سیستم ایمنی اتفاق میافتد، عملکرد سایر سیستمهای فیزیولوژیک بدن را هم تحتتاثیر قرار میدهد. دکتر Fagarasan اولین بار در سال ۲۰۰۲ عنوان کرده است که احتمال دارد IgA بیشتر از اینکه میکروبها را نابود کند، به کمک برخی از آنها بیاید.
مقالهی مرتبط: آنتیبادی مهندسیشده جدید میتواند ۹۹ درصد از ویروسهای HIV را نابود کند
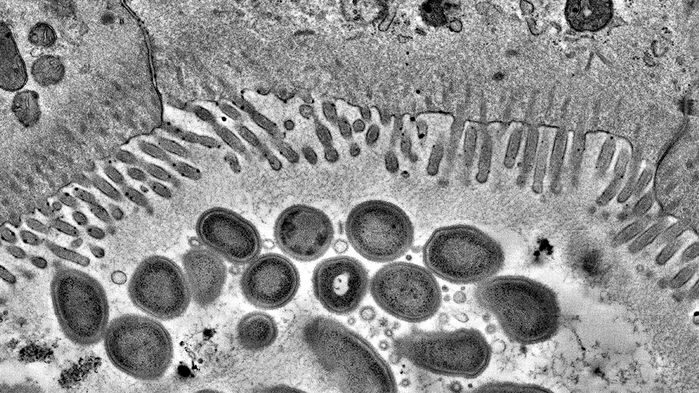
IgA حدود ۵۰ سال پیش کشف شده است. هر فرد در یک روز ۳ تا ۵ گرم از این آنتیبادی تولید میکند که این مقدار حدود ۷۵% کل آنتیبادی تولیدی بدن را تشکیل میدهد. IgA در شیر مادر نیز فراوان است و با عفونتهای مختلف نوزاد مقابله میکند.
پس از اینکه محققان فهمیدند موشهایی که مقدار IgA بدنشان کمتر است، میکروبیومهای غیرطبیعی دارند، دکتر Fagarasan پیشنهاد داد شاید IgA در نگهداری و کنترل باکتریهای بدن نقش داشته باشد. تاکنون مکانیسم یا روشی برای اثبات این فرضیه وجود نداشته است اما به تازگی شواهدی برای این موضوع پیدا شده است.
در مجتمع تکنولوژی کالیفرنیا در Pasadena، میکروبیولوژیست Sarkis Mazmanian و شاگردش Gregory Donaldson روی گونهی خاصی از باکتریهای بدن تحقیق کردهاند. آنها تلاش کردند تا بفهمند Bacteroides fragilis چگونه میتواند مدتهای طولانی بدون تغییر در رودهی انسان باقی بماند. این باکتری میتواند به کاهش عوارض کولیت، مالتیپل اسکلرزیس و حتی اوتیسم کمک کند.
Donaldson با استفاده از تکنیکهای مختلف ایمونولوژیکی، میکروبیولوژیکی، ژنتیکی و تصویربرداری، فهمید که برای وجود پایدار باکتری در روده، IgA ضروری است. Donaldson و همکارانش طبق تحقیقات دریافتند این باکتری سطحش را با قندهایی که در مقیاسهای بزرگ به IgA وصل میشوند، میپوشاند.
IgA اغلب به این دلیل به پاتوژنها وصل میشود تا آنها را غیرمسلح کرده و حذف و پاکسازی آنها را سرعت بخشد. اما در مورد باکتری Bacteroides fragilis، اتصال IgA باعث میشود باکتریها در مخاط روده به یکدیگر وصل شوند و لایهی موکوسی محافظ مخاط روده را سوراخ کنند. با این اتفاق باکتریها میتوانند به سلولهای مخاطی دسترسی پیدا کنند. محققان گزارش دادهاند بدون وجود IgA میکروبها نمیتوانند در روده برای مدت طولانی تکثیر شوند.
Donaldson در ادامه گفته است:
این چیزی نیست که ما انتظار داشتیم؛ یک مولکول خاص از سیستم ایمنی میتواند اثرات متفاوتی روی گونههای باکتریایی متفاوت بگذارد.
مقالهی مرتبط: شاید بیماری خود ایمنی لوپوس، محرک باکتریایی داشته باشد
مهمترین آزمایش دربارهی نقش IgA، روی موشهایی که در محیطی کاملا ایزوله و فاقد میکروب رشد داده شده بودند، انجام شده است. برخی از این موشها از نظر ژنتیکی تغییر داده شده بودند تا نتوانند IgA تولید کنند. طبق گزارشات زمانی که Bacteroides fragilis به رودهی موشهای دارای IgA اضافه میشد، میتوانست در آنجا ساکن شده و تکثیر یابد اما در موشهای فاقد IgA، این باکتری قادر به ساکن شدن نبود.
Donaldson خاطرنشان کرده است احتمالا چندین نوع باکتری دیگر نیز وجود دارند که برای تکثیر و کلونیزه شدن در روده نیاز به IgA دارند. زمانی که میکروبیوم طبیعی موشها به رودهی موشهای بدون میکروبی که نمیتوانستند IgA بسازند منتقل شد، چندین نمونه از اجزای این میکروبیوم نمیتوانستند در روده ساکن شده و در آن باقی بمانند.
طبق اظهارات Mazmanian، این موضوع نشان میدهد ما تا چه اندازه به زندگی در کنار میکروبیوم بدنمان عادت کردهایم! با این تحقیقات زیربنای همزیستی تا حدودی مشخص خواهد شد.
Fagarasan افزوده است نتایج این تحقیقات از این فرضیه حمایت میکند که IgA نه تنها برای مقابله با پاتوژنهای مهاجم، بلکه برای کمک به فلور رودهای ما بوجود آمده است.
Nicholas Mantis ایمونولوژیستی از دپارتمان سلامت مرکز Wadsworth در نیویورک، نیز معتقد است آنتیبادیها به عنوان چارچوبی برای باکتریها عمل میکنند. باکتریها با استفاده از این چارچوب بهتر میتوانند به موکوس بچسبند. وی هنوز در اینباره که باکتریها برای اطمینان از اتصال IgA، ساختارهای خاصی را در سطحشان ایجاد کرده باشند، مردد است.
پزشکان میتوانند از این نتایج برای درمان بیماریهایی که در آنها میکروبیوم رودهای از کار میافتد یا دفع میشود استفاده کنند. Mantis معتقد است استفاده از آنتیبادیها در چنین بیماریهایی میتواند به ثابت کردن و استقرار باکتریهای مفید در روده کمک کند. این تکنیک احتمالا در آینده به یکی از روشهای درمانی پرکاربرد طولانیمدت تبدیل خواهد شد.
