مولکولها آن طور که ما فکر میکردیم، رفتار نمیکنند. این کشف میتواند انقلابی در شیمی به پا کند.
یکی از نمایشگاههای موزهی علم لندن، یک بار پر از توپ است. اگر در گالریهای همکف قدم بزنید یک راهپله در سمت راست میبینید. در یک جعبهی شیشهای دراز، همراه با یک ماشین آتشخاموش کن قدیمی، یک دستگاه حفاری میبینید.
این نمایشگاه، داستان ساخت دنیای مدرن را نقل میکند و مخصوصاً این یکی، یکی از انقلابیترین توسعهها را نشان میدهد. این مدلی است که دوروتی هوجکینِ شیمیدان از پنیسیلین، اولین آنتیبیوتیک کشف شده، ساخت. توپهای رنگارنگی که با چوب به هم وصل شدهاند، آرایش سهبعدی اتمها را در داخل مولکول نشان میدهد؛ رازی که به ما قدرت تولید انبوه این مولکول و نجات جان میلیونها انسان را داد.
مشاهدهی منسوخ شدن این مدل، در دنیایی که ابر رایانهها میتوانند با دقت بالا پیکربندی اتمها را تعیین کنند، کار دشواری نیست. ولی این تنها خود مدل نیست که جایش در موزه است؛ به نظر میآید کل مفهومی که ما از مولکول در نظر داریم، به زودی به تاریخ خواهد پیوست. باید فراتر از این گوی و میلهها را دید، و این دیدگاه میتواند شیمی را متحول کند، کشف داروهای جدید را سرعت بخشد و ما را در تولید موادی که دنیا به آنها وابسته است، باهوشتر و سریعتر سازد.
برای درک اهمیت دست بردن در مولکولها، فقط کافی است به کاور گوشی یا نوشتههای روی تیشرتتان نگاه کنید. به سختی میتوان حوزهای از زندگی امروزی را یافت که بر اتصال سادهی مولکولها به هم برای ساخت انواع جدیدتر و جالبتر از آنها تکیه نداشته باشد. با این حال، داستان پنیسیلین خیلی کلاسیکتر، این قدرت را به نمایش میگذارد.
در طول جنگ جهانی دوم، شیمیدانان این دارو را با کشت کپک در ماهیتابه تولید کردند! آزمایشگاهها این ظروف را حتی در سقفها هم گذاشته بودند ولی این پروسه هنوز هم مقدار کمی دارو در اختیارشان قرار میداد. توزیع این ماده تا حدی محدود بود که ترکیبات متابولیزهنشده را از ادرار سربازان جمع میکردند و مورد بازیافت قرار میدادند. برای نائل شدن به راهی بهتر، قبل از هر کاری باید ترکیب دارو را مشخص میکردیم؛ اتمها چگونه به هم متصل شده بودند؟
در این نقطه بود که هوجکین و مدلش ظاهر شدند. او این کار را با تاباندن پرتو ایکس و تفسیر الگوهای ایجاد شده انجام داد. در سال ۱۹۴۵ او مدلی را ساخت که اکنون در موزهی علم لندن قرار دارد. شیمیدانان پس از این به فکر تولید انبوه آن افتادند. کاری که در نهایت، جان شیهان، سال ۱۹۵۷ در MIT از عهدهی آن برآمد.
حتی خود هوجکین و شیهان هم میدانستند که مولکولها، گوی و میلههای مینیاتوری نیستند. ما از خیلی وقتها پیش میدانیم که پیوندها کش میآیند و اتمها لرزش دارند. اتمها حتی میتوانند با حیلههای کوانتومی ناپدید و دوباره ظاهر شوند؛ کارهایی که گوی و میلههای بیچاره از انجام آن عاجزند.
ولی این مدل ساده به طرز اعجابانگیزی خوشدست بود. از حق نگذریم، همهی واکنشهای شیمیایی با شکستن پیوندهای کوالانسی (میلهها) و جوش خوردن دوبارهی آنها توجیه میشد. این پیوند چیزی بیشتر از دو الکترون که بین اتمها به اشتراک گذاشته شدهاند، نیست. بعضی اوقات این پیوندها جدا شده و هر اتم یک الکترون میگیرد و رادیکالهای بسیار واکنشپذیر به وجود میآیند. ولی اکثر اوقات، دقیقاً قبل از از هم پاشیدن مولکولها، پیوندها قبل از شکست نهایی، تا وضعیت بسیار فشردهای کشیده میشوند، پیوندهای جدیدی تشکیل میدهند و مولکولهای جدیدی میسازند.
این وضعیت کنترل بین مولکول اولیه و فرآورده، وضعیت انتقال نام دارد؛ وضعیتی که مولکولها اصلاً دوست ندارند در آن بمانند؛ چون انرژی زیادی برای رسیدن به آن نیاز است. به یک سرسره میماند، برای لذت بردن از سر خوردن، اول باید پلهها را بالا بروید. نظریهی وضعیت انتقال میگوید اگر بدانید گوی و میلهها در این سه وضعیت به چه شکل هستند، میتوانید تبادل انرژی را بعد از رسیدن به وضعیت انتقال و گذر از آن حساب کنید. این کار سرعت واکنش را به شما خواهد گفت که برای ساخت آن مولکول در آزمایشگاه ارزشمند و ضروری است. هر آنچه که برای یک پیشبینی دقیق نیاز دارید، محل اتمها است.
شیمیدانها دلشان نمیآید به این مدل خیانت کنند: نظریهی ساده و شهودی که همیشه جواب میدهد. تا این که … دیگر جواب نداد.
در سال ۲۰۰۴، شایعاتی در محافل آکادمیک از این گوش به آن گوش میرسید، مبنی بر این که برخی واکنشها وضعیتهای انتقال عجیبی دارند که این نظریه را خدشهدار میکند. یکی از آنها تجزیهی فرمالدهید (یک کربن متصل به یک اکسیژن و دو هیدروژن) بود. آیا یک استثناء میتوانست از چشمها پنهان بماند؟
این ایده نظر آرتور سوتز، شیمیدان دانشگاه استونی بروک نیویورک را جلب کرد. او میدانست که برای پیشگام بودن در حل این مشکل باید سریع عمل کند، ولی در همان حین آماده میشد تا در دانشگاه دیگری در آن سوی کشور استخدام شود. در شلوغ پلوغیهای آزمایشگاه، او و تیمش مولکولهای منفرد فرمالدهید را ایزوله کردند تا تجزیهی آنها را به کربنمونوکسید و هیدروژن مشاهده کنند. تجهیزات او این اجازه را میداد تا COها را به دام بیندازند و انرژی آنها را اندازه بگیرند. این کار اجازهی پیشبینی انرژی مولکولهای هیدروژن را نیز میداد؛ فقط کافی بود انرژی CO را از انرژی فرمالدهید کم کرد.
“هیچ چیز تا آخرین لحظه معلوم نبود. ما تمام شب را در آزمایشگاه ماندیم. آزمایش ما جواب داد. معلوم شد که مولکولهای CO به طور باورنکردنیای آرام میچرخند. این به آن معنا بود که مولکولهای هیدروژن باید انرژی عظیمی میداشتند؛ انرژیای که برای تجزیهی آنها تقریباً کافی بود. این با تصورات ما همخوانی نداشت”.
سوتز، جوئل بومن، شیمیدان دانشگاه اموری آتلانتا را که برای همین واکنش یک شبیهسازی کامپیوتری توسعه داده بود، از نتایج آزمایش باخبر کرد. بومن، تکهی دیگر پازل، رفتار با جزئیات هیدروژن، را مشاهده کرد. نتایج او هم با محاسبات سوتز همخوانی داشت.
در شبیهسازی بومن، اتمهای هیدروژن به طور دیدنی از رفتار طبیعی خود سرپیچی میکردند. به جای وارد شدن به وضعیت انتقال، به نظر میآمد یکی از اتمهای هیدروژن قبل از تشکیل یک مدار دور آن از باقی مولکول دور میشود، در نهایت به بقیهی مولکول در طرف دیگر میپیوندد و به هیدروژن دیگری ملحق میشود.
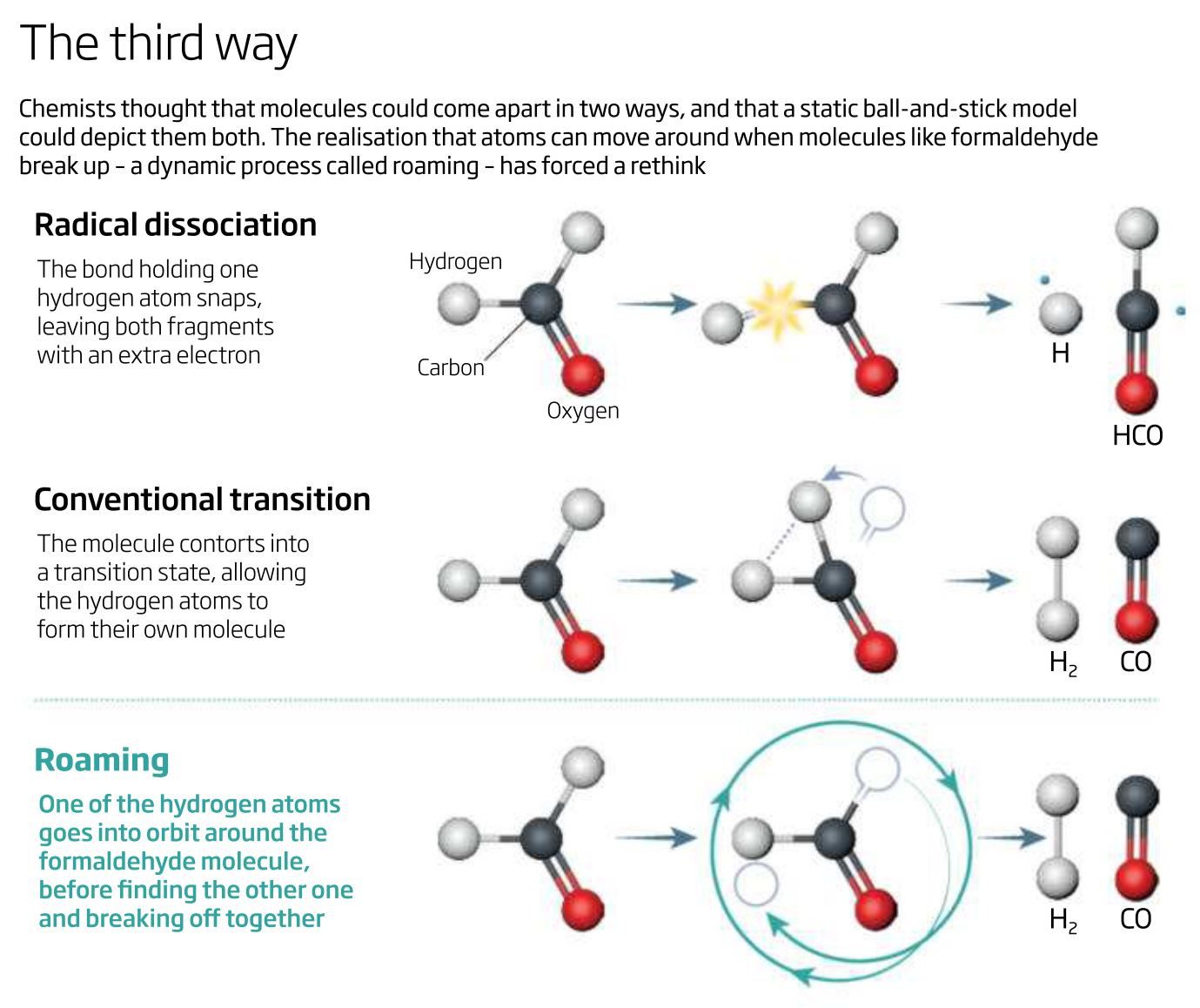
این واکنش به هیچ کدام از مشاهدات قبلی شبیه نبود. به جای وضعیت انتقال متعارف یا جدایی رادیکال، به نظر میآید فرمالدهید راه سومی را برای تجزیه انتخاب میکند: به یکی از اجزای تشکیلدهندهاش اجازهی پیادهروی میدهد (شکل را نگاه کنید). بومن میگوید:
“ما دربارهی واژهی مناسب بسیار فکر کردیم. در نهایت به کلمهی “roaming” (به معنای پرسه زدن) رسیدیم”.
به زودی ما رومینگ را در پنج ترکیب سادهی دیگر مشاهده کردیم که بیش از پیش محدودیتهای روش استاتیک گوی و میله را به رخمان میکشید. تحرکات کوتاهی که شیمیدانان برای دههها آنها را نادیده میگرفتند، چون فکر میکردند چیز مهمی نیست، اکنون به موضوع مورد علاقه تبدیل شده است. اگر جنبش اتمها مورد توجه قرار نگیرد، شیمی ناقص میماند. باید دربارهی تفکرمان درمورد ماهیت و چگونگی وقوع واکنشها تجدید نظر کنیم.
چهارده سال میگذرد، ولی همه رومینگ را به عنوان یک تحول بنیادین نمیبینند. دیوید گلوواکی، شیمیدان دانشگاه بریستول انگلستان اعتقاد دارد “صحبتهای زیادی راجع به رومینگ انجام شده است”. او به این نکته اشاره میکند که به جز یکی دو تا مقالهی پر بحث، شیمیدانها این مکانیسم را فقط در شرایط نزدیک به خلأ دیدهاند. منتقدان دربارهی وقوع این مکانیسمها در چیزهایی که برای ما اهمیت دارند، سؤال میپرسند؛ مثلاً در مایعات، چون فازی است که بیشتر واکنشهای جهان در آن رخ میدهد.
شیمی در جنبش
با این حال، در چند سال گذشته، نمونههای بیشتری از این جنبشهای مولکولی کشف شده که مطابق پیشبینیهای نظریهی متعارف وضعیت انتقال عمل نمیکنند. اینها شامل واکنشهای در فاز مایع هم میشود که شیمیدانها برای ساخت مواد از آن استفاده میکنند. دن سینگلتون از دانشگاه Texas A&M میگوید که “این حوزه در حال گسترش است”. او چند مورد از چنین مکانیسمها را کشف کرده و آنها را اثر دینامیک مینامد.
سالها پیش، شیمیدانان اعتقاد داشتند که مولکولهایی که وارد وضعیت انتقال میشوند فقط یک راه خروج دارند، و همواره همان فرآوردهها را تولید مینمایند. یکی از مکانیسمهایی که سینگلتون شناسایی کرده، این منطق را کنار میزند. به مولکولی فکر کنید که از نردبان سرسره بالا میرود، ولی برای سر خوردن نه یک راه، بلکه چندین راه دارد. با تغییر شرایط، سرسرههای متفاوتی ترجیح داده میشوند و این یعنی، مولکولهایی در وضعیت انتقال یکسان میتوانند در آخرین لحظه مسیرهای مختلفی به سمت پائین بپیمایند. در نتیجه، در پایان واکنش شما با نسبتی از فرآوردهها در ظرف مواجهید و این با چیزی که نظریهی انتقال پیشبینی میکند همخوانی ندارد.
مقاله مرتبط: مهندسی مولکولی: دریچهای رو به دنیایی جدید
این مشکلات از حد آزمایشگاه فراتر میرود. دین تانتیلو در دانشگاه کالیفرنیا، دیویس، محاسبه کرده که اثرات دینامیک در ساخت مواد فراری به نام ترپن در گیاهان نیز دخیل است؛ بعضی از این مواد مسئول بوی جنگلها هستند. در این مورد، چندین سرسره در مسیر واکنش کمک میکند تا با یک واکنشدهنده، طیف وسیعی از مولکولها تولید شوند.
از همهی اینها چه نتیجهای میتوان گرفت؟ ساختار گوی و میله تصویر خوبی است ولی دیگر از مُد افتاده است. مولکولها دائماً در حال جنبش اند و فکر کردن به پیوندها به عنوان اتصالات سفت و سخت بین اتمها درک شهودی واکنشهای شیمیایی را دشوار میسازد.
اگر ما به کارکرد اثرات دینامیک پی ببریم، شاید قادر باشیم آنها را برای طراحی واکنشهای بهتر مهار کنیم و اگر نوع جدیدتری پیدا کنیم، شاید بتوانیم سریعتر به سنتز بپردازیم. شاید حتی به راه جدیدی برای ساخت دارو دست یابیم.
مشکل این است که بدون نظریهی وضعیت انتقال، به راههای جایگزینی برای توجیه واکنشها نیاز داریم. استیون ویگینز، ریاضیدان دانشگاه بریستول، باور دارد که به خال زده است. او به همراه گلوواکی و دیگران یک سرمایهی چهار میلیون پوندی از شورای تحقیقاتی انگلستان دریافت کردهاند تا راههای نمایش دادن شیمی دینامیک را مورد بررسی قرار دهند.
اولین قدم، ایجاد ساختارهایی برای مولکولهاست که استاتیک نباشند، بلکه حرکت اتمها را هم حساب کنند. این یعنی توصیف هر اتم نه فقط با اتصالاتش در فضای سه بعدی، بلکه همراه با سرعت و جهت حرکت آنها.
مشکل این است که با این کار، اطلاعات لازم برای توصیف مولکول در هر لحظهی معین دو برابر میگردد و شبیهسازی کامپیوتری باید وارد کار شود. بدتر از همه این است که اگر شرایط اولیه کمی عوض شود، مدل پیچیدگیای دارد که میتواند نتایج را به کلی تغییر دهد. خلاصه، هیچ کس کاملاً نمیداند که این راهحلها با معنای واقعی شبیهسازی چه مشکلی ایجاد میکنند.
ویگینز شروع به حل این مشکل کرده است. او با استفاد از الگوریتمهای یادگیری ماشینی در نظر دارد از یک دریای اطلاعات الگوهایی را شکار کند که میتوانند مسیر پیشرفت واکنش را پیشبینی کنند. احتمالات بیشماری وجود دارد. اگر چگونگی تعیین راه واکنش توسط ارتعاشات مولکولی را درک کنیم، کسب مزیت کردهایم. ما میتوانیم واکنشها را به مسیرهای دلخواهمان هدایت کنیم تا مواد شیمیایی مورد نظرمان را به دست آوریم. متناوباً، شاید واکنشهایی را شناسایی کنیم که هرگز تاکنون تصور نکرده بودیم. این برای سنتز شیمیایی کاربرهای فراوان دارد. سینگلتون در این باره نظر جالبی دارد:
“این چالش بسیار دشواری است. من راجع به موفقیت آنها مثبت نمیاندیشم، ولی آنها کار درست را برای امتحان کردن انجام میدهند”.
مدل ویگینز (ترکیبی از کدهای رایانهای و ریاضیات پیچیده) شاید از لحاظ زیباییشناختی به پای مدل گوی و میلهی موزهی علم لندن نرسد. ولی اگر این آرزو تحقق یابد، بازطراحی آنها از شیمی شاید جایی بهتر در موزه برای آنها باز کند.
مقاله مرتبط: تئوری جدید تکامل مولکولی
دانشمندان مولکولی ساختهاند که شاید پارادوکس منشأ حیات را حل کند