مصرف آنتیبیوتیک میتواند رشد باکتریها را افزایش دهد.
گروهی از محققان دانشگاه اکستر بریتانیا (University of Exeter) در یک مطالعۀ جدید، باکتری اشریشیا کلی (E. coli) را طی ۴ روز و در ۸ مرحلۀ درمانی متوالی در معرض آنتیبیوتیک قرار دادند؛ مشاهده شد که باکتریها در هر مرحله به میزان بیشتری [نسبت به مرحۀ قبل] در برابر آنتیبیوتیک مقاومت حاصل میکنند.
البته این نتیجه چندان هم غیرمنتظره نیست؛ اما بخش غافلگیرکنندۀ ماجرا سرعت تولیدمثل سرسامآور باکتریها جهشیافته بود، به گونهای که این باکتریها توانستند جمعیتهایی تا ۳ برابر بزرگتر [از حد معمول] تولید کنند (در حقیقت این جهشها باعث ایجاد مقاومت در باکتریها شده بود). این پدیده تنها در باکتریهایی مشاهده شد که در معرض آنتیبیوتیک قرار گرفته بودند. محققان در ادامه با حذف آنتیبیوتیک از محیط، مشاهده نمودند که تواناییهای مقاومتی جدیدالحصول غیرقابل بازگشت بوده و در باکتریهای میزبان حفظ میشود.
پروفسور رابرت بیردمور (Robert Beardmore)، استاد دانشگاه اکستر و سرپرست این مطالعه، در این باره میگوید:
نتایج مطالعات ما نشان میدهد که حصول مقاومت نسبت به سطوح کلینیکی آنتیبیوتیکها در باکتری E. coli، مزایای زیادی برای این باکتری به ارمغان میآورد. اغلب گفته میشود که تکامل داروینی فرآیندی آهسته است؛ اما هیچ چیزی به اندازۀ این ادعا از حقیقت فاصله ندارد، علیالخصوص هنگامی که باکتریها در معرض آنتیبیوتیک قرار بگیرند. باکتریها توانایی خارقالعادهای در تغییر دادن DNA خود دارند و همین قضیه میتواند در عرض چند روز، داروی مورد استفاده را سرکوب نماید. با این که تغییر سریع DNA، پدیدهای خطرناک [حداقل] برای انسان محسوب میشود؛ ولی برای باکتریهایی مثل E. coli – به شرط مساعد بودن تغییرات – بسیار سودمند است.
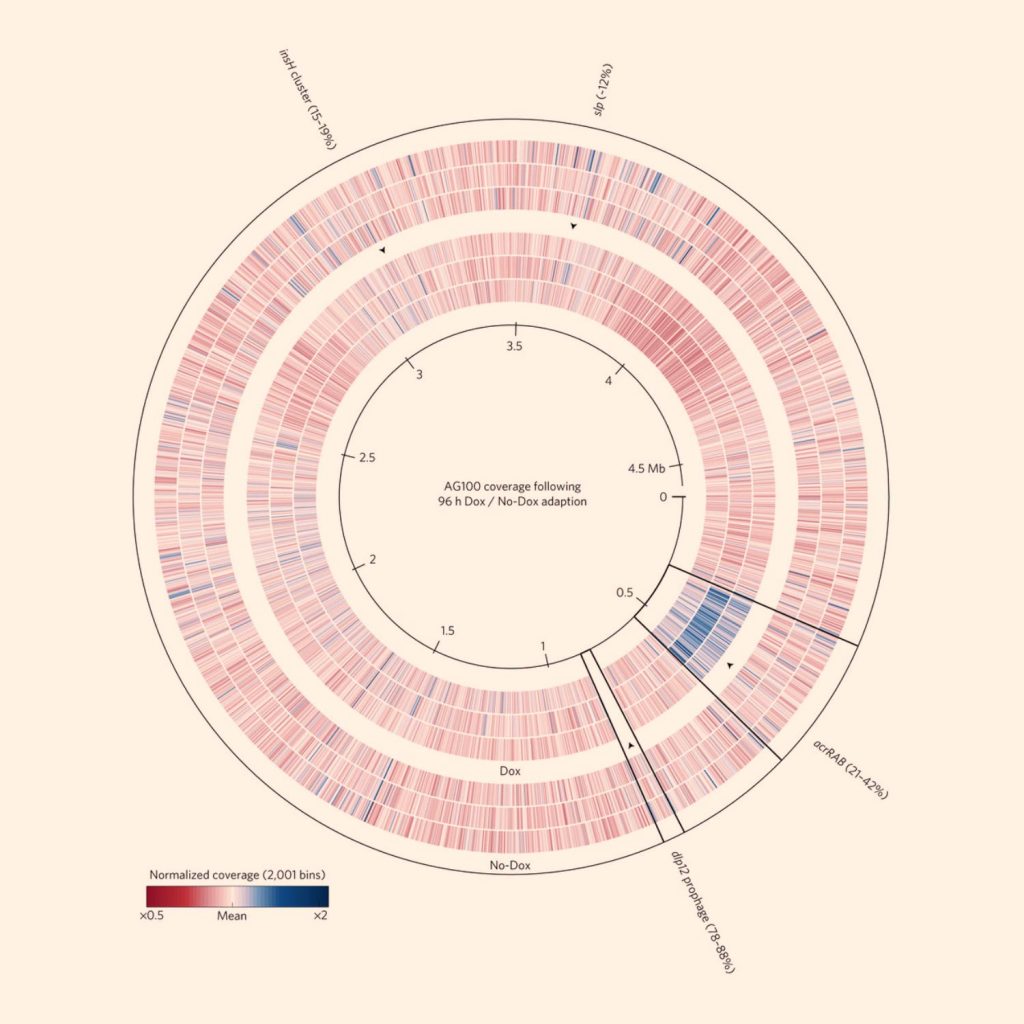
پروفسور بیردمور و همکارانش به عنوان بخشی از مطالعۀ خود بر روی تغییرات ژنتیکی ناشی از برخورد با آنتیبیوتیک در باکتریها، تأثیرات داروی داکسیسایکلین (Doxycycline، آنتیبیوتیک) بر E. coli را مورد ارزیابی قرار دادند.
باکتریهایی که طی مطالعه تکامل حاصل نموده بودند در دمای منفی ۸۰ درجه منجمد شدند تا تغییرات صورت گرفته در DNAشان بررسی شود. پارهای از تغییرات ژنتیکی به خوبی شناسایی و در بیماران کلنیکی نیز مشاهده شدهاند؛ مانند بیان تعداد بیشتری از پمپهای غشایی مسئول دفع آنتیبیوتیک؛ که باکتری را در برابر داروی مذکور مقاوم میکند. تغییر دیگری نیز که مشاهده شده است، از دست رفتن بخشی از DNA باکتریایی است که منشأ ویروسی دارد.
گروه تحقیقاتی این یافته را چنین توصیف میکند:
به نظر ما از دست دادن DNA ویروسی با جلوگیری از بروز مرگ سلولی در E. coli، منجر به افزایش سرعت تقسیم بیرویۀ این باکتری در پی بیان تعداد بیشتری از پمپهای غشایی میشود. معمولاً پدیدۀ خودکشی (مرگ سلولی برنامهریزی شده) در E. coli منجر به تولید زیستلایه (Biofilm، اجتماعی از میکروارگانیسمهای متصل به هم که به سطوح میچسبند) میشود و همین قضیه به باکتریها کمک میکند تا بتوانند بر روی سطوح مستقر شوند. شما میتوانید این زیستلایهها را در سینک ظرفشویی مشاهده نمایید. ولی ما در مطالعۀ خود از محیط مایع – شبیه به جریان خون – استفاده نمودیم. این مسئله باعث عدم تولید زیستلایه و در نهایت افزایش سرعت تقسیم سلولی میشود. گفته میشود که مقاومت آنتیبیوتیکی در صورت استفاده از دوزهای بالا روی نمیدهد، ولی نتایج مطالعۀ ما نشان داده است که باکتریها میتوانند در شرایط مختلف تغییر نمایند؛ که این قضیه در درمان بعضی از عفونتها مطلوب واقع نخواهد شد. این مطلب بدین معنی است که هنگام درمان بیماریهای عفونی باید آنتیبیوتیک مناسب با سرعت هرچه تمامتر برای بیمار تجویز شود تا چنین سازگاریهای در باکتری عامل بیماری حاصل نشود.
