چاقی یک وضعیت پزشکی است که در اور عدم توازن در جذب و دفع انرژی، چربی زیادی در بافت چربی تجمع میابد. طبق نظرسنجی سازمان ملی بهداشت و تغذیه، بیش از یک سوم (~۳۴.۹%) بزرگسالان در ایالات متحده آمریکا سال ۲۰۱۲-۲۰۱۱ چاق بودند. چاقی ارتباط تنگاتنگی با اختلالات متابولیکی، شامل دیابتها، هیپرلیپیدمی، اختلال کبد چرب غیرالکلی، فشارخون بالا و اختلالات قلبی عروقی و همچنین طیف گستردهای از سرطانهای کبد، پروستات، پستان و روده بزرگ دارد. هزینههای پزشکی مرتبط با چاقی در ایالات متحده بیش از ۱۵۰ میلیارد دلار در هر سال است.
چاقی به علل ژنتیکی در خانوادهها ریشه میدواند. با این حال، رژیم و سبک زندگی افراد خانواده در آن تاثیر میگذارد. رژیم و سبک زندگی دو فاکتوذ محیطی مهماند که با شیوع چاقی درارتباطاند. رژیمهای غذایی پرچرب (HFD)، به دلیل طعم و مزهای که دارند، معمولا انرژی بیشتری از آنچه بدن نیاز دارد دریافت میکنند و در صورت عدم تحرک فیزیکی کافی درنهایت منجر به چاقی میشوند.
از نظر بیوشیمیایی چاقی یک وضعیت فیزیولوژیکی است که در آن ذخیره چربی بیش از حد مورد نیاز است. علت آن فرایندهای بیوشیمیایی درگیر در آنزیمها و ژنهای مسئول نگهداری هوموستاز است. اگر واکنشهای بیوشیمیایی که به نفع سنتز و تجمع چربیاند بیش از فرایندهای شیمیایی مسئول تامین انرژی باشد، چاقی شکل میگیرد. ازآنجاییکه تجمع لیپید و مصرف آن از عملکردهای مخصوص گروه پروتئینهایی است که از DNA کد میشوند، نقوص ژنتیکی در کد کردن توالیها یا تنظیم توالیها برای بیان آنها، پایه چاقی را شکل میدهد. استراتژیهای فعلی در درمان یا پیشگیری چربی متمرکز بر مسدود کردن تجمع لیپیدها و یا افزایش میزان مصرف انرژی است. رویکرد ژندرمانی متمرکز بر انتقال توالیهای کدکننده یا غیرکننده ژن برای تولید پروتئینهای ضروری و حیاتی بازسازی کننده و نگهداری کننده متابولیک هوموستاز است.
مقالات مرتبط: آیا بالاخره زمان ژن درمانی رسیده است؟
ژنهایی که نقش حیاتی در چاقی دارند
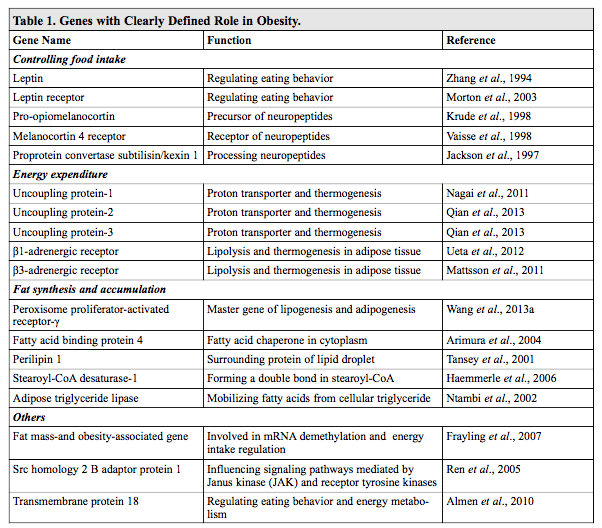
هوموستاز متابولیک نیاز به فعالیت هماهنگ و متقابل از ژنهای متعدد از جمله ژنهای کدکننده پروتئین/آنزیم مسئول دریافت غذا، لیپوژنز، لیپولیز، متابولیسم گلوکز و ذخیره جربی در بافت چربی است. ژنهایی که بیان این ژنهای ضروری را تنظیم میکنند نیز نقش مهمی در تعیین فرایندهای متابولیک دارند. زمانیکه انرژی اضافی باشد، بیان بیش از حد یا کمتر از حد یک یا چند ژن حیاتی هوموستاز متابولیک نیز میتواند منجر به چاقی شود. برای مثال، موشهایی که کمبود لپتین یا رسپتور آن در مغز را دارند، معمولا چاق هستند و عوارض شدیدی دارند. انواع ژنتیکی برای ژنهای پرواپیوملانوکورتین (POMC)، مبدل پروپروتئین subtilisin/kexin 1 (PCSK1) و ملانوکورتین ۴رسپتور (MC4R)، دلیل اصلی ۵% از موارد چاقی مفرط در مراحل اولیه رشد کودکیاند. به همین ترتیب، چاقی پلیژنیک عمدتا به علت اثرات افزایشی یا همافزایی ژنهایی است که به طور انحصاری برای عدم توازن هوموستاز کافی نیست. مطالعات اخیر بسیاری از ژنهای مسبب چاقی را مشخص کردهاند که برخیشان در جدول زیر آورده شده است.
لپتین، بیشترین ژن با ارتباط مستقیم در چاقی است، که نقش کلیدی در تنظیم دریافت انرژی و تاثیر بر اشتها و گرسنگی دارد. این یکی از مهمترین هورمونهای مشتق شده از چربی است. عملکرد لپتین با اتصال به گیرنده لپتین در مغز برای کنترل حس گرسنگی عمل میکند. موشهای هموزیگوت به خاطر جهش ob (ob/ob) دچار تغذیه و چاقی شدید میشوند. همانند لپتین، POMC با تولید خوشهای از فاکتورهای اصلی همچون ملانوکورتین پپتیدها آدرنوکورتیکوتروپین (ACTH)، هورومونهای تحریک کننده ملانوسیت آلفا (MSH)، بتا و گاما، همچنین گیرنده اپیویید لیگاند بتا-اندروفین، نقش مهمی در تنظیم غذای دریافتی دارند. یک نقص ژنتیکی در ژنهای POMC مرتبط با ایجاد شروع زودهنگام چاقی شدید است. مبدل پرو-پروتئین subtilisin/kexin 1 (PCSK1) یک آنزیم ضروری مورد نیاز در پردازش پس از انتقال POMC است، همچنین نقص ژن PCSK1 منجر به چاقی میشود. پس از اینکه POMC توسط PCSK1 پردازش شد، MSH به رسپتورش یعنی MC4R متصل میشود تا عملکرد آن را در کنترل مصرف غذا کنترل کند. یک جهش تغییر چهارچوب در MC4R مرتبط با چاقی، به طور عمده به ارث میرسد. ژنهای بالا در تنظیم رفتار خوردن به طور کلی کار میکنند ونقص در هر یک از آنتا به چاقی شدید در انسان منجر میشود.