اکثریت مبتلایان به سرطانهای ریهی کشنده را (۸۵ درصد)، کارسینوم غیر سلول کوچک ریه (NSCLC) تشکیل میدهد. این کارسینوم اغلب دارای ژن جهش یافتهای تحت عنوان LKB1 است. محققان انستیتو Salk، چگونگی منجر شدن LKB1 غیر فعال به ایجاد سرطان را به دقت کشف کردهاند. نتایج شگفت آوری که در نشریه Cancer Discovery منتشر شدهاست، چگونگی ارتباط میان LKB1 و دو آنزیم، که در سرکوب التهاب و رشد سلولی نقش دارند، در جلوگیری از رشد تومور آشکار میسازد. این یافتهها میتوانند به درمانهای جدیدی برای NSCLC منجر شوند.
پروفسور روبن شاو، مدیر مرکز سرطان Salk و مولف ارشد این مطالعه میگوید: “برای اولین بار، ما اهداف مستقیم و مخصوصی برای LKB1 که از سرطان ریه جلوگیری میکند، یافتهایم و به طرز غیر منتظرهای دریافتیم التهاب در رشد این تومور، ایفای نقش میکند. با این اطلاعات ما میتوانیم درمانهای جدیدی برای این دستهی عظیم از بیماران مبتلا به سرطان ریه ایجاد کنیم.”
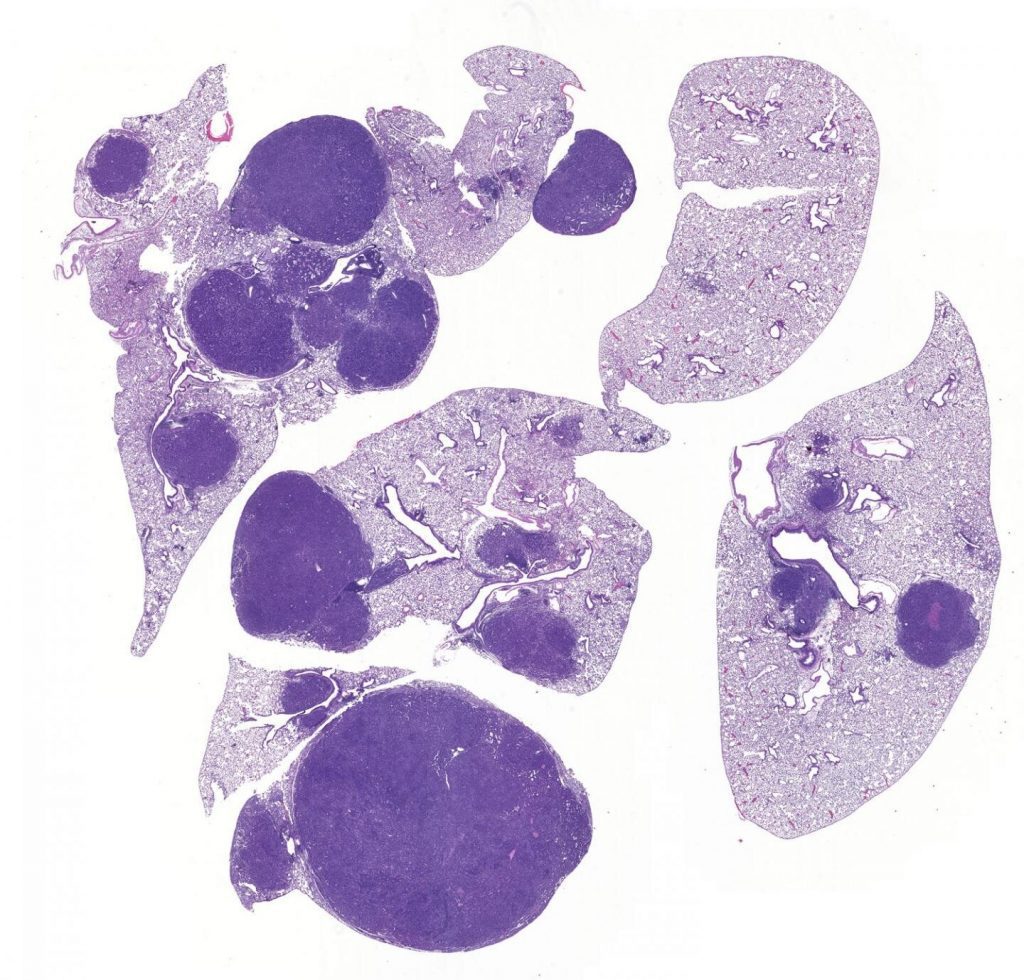
LKB1 زمانیکه بصورت طبیعی فعالیت میکند، بعنوان یک سرکوبگر تومور ظاهر میشود و فعالانه از تشکیل سرطان در مراحل اولیه، جلوگیری میکند. دانشمندان میدانستند ژن LKB1 بعنوان کاپیتان یک تیم انتقال سیگنال که سیگنالهای سلولی را به آنزیمهایی تحت عنوان کیناز انتفال میدهند، فعالیت میکند. LKB1 بعنوان هماهنگ کننده ۱۴ کیناز مختلف، ایفای نقش میکند. ولی اینکه کدام یک از این کینازها مسئول عملکرد سرکوبگری تومور LKB1 است، نزدیک به ۱۵ سال از شناسایی اولیه LKB1 بعنوان یک ژن مختل شدهی عمده در سرطان ریه، ناشناخته بودهاست. در سال ۲۰۱۸، آزمایشگاه شاو، با نشان دادن اینکه ۲ مورد از ۱۴ آنزیم بطرز شگفت انگیزی در اثرات LKB1 در جلوگیری از سرطان ریه مهم نیستند، اولین گام را در حل کردن این معمای مولکولی برداشت. تقریبا هیچ اطلاعاتی در مورد ۱۲ کیناز باقیمانده که همگی مهم بودند، در دسترس نبود.
پابلو هولشتاین، مولف اول این مطالعه اذعان دارد: “این، مانند یک مورد کارآگاهی سرطان بود. ما به نقش داشتن یکی از این ۱۲ کیناز بعنوان عامل کلیدی در اثرات سرکوبگری تومور LKB1 شک داشتیم.”
بمنظور برطرف کردن این شک، تیم از تکنولوژی CRISPR در کنار آنالیز ژنتیکی بمنظور غیر فعال کردن هر یک از کینازهای مربوطه به تنهایی و سپس بصورت دسته جمعی بهره بردند. آنها، نحوهی تاثیر این غیر فعالسازیها بر ایجاد و رشد تومور در سلولهای NSCLC و مدل موشی NSCLC را مطالعه کردند. این بررسی، دو کیناز را به محققان نشان میداد: یکی تحت عنوان SIK1 که قویترین اثر را در متوقف ساختن تشکیل تومورها داشت. زمانیکه SIK1 غیر فعال میشد، رشد تومور افزایش مییافت؛ و زمانیکه SIK3، یک کیناز مرتبط، نیز غیر فعال میشد، تومور بصورت تهاجمیتری رشد میکرد.
شاو میگوید: “کشف اینکه SIK1 و SIK3، مهمترین کینازها از میان آن ۱۴ آنزیم هستند، مانند یک کشف یک بازیکن ناشناخته بسکتبال است که تقریبا هیچ موقع بازی نمیکند ولی یکی از مهمترین بازیکنان در تاریخ ورزش است.”
بیشتر بخوانید: https://virtualdr.ir/2016/11/01/lung-cancer-part-1/
همچنین LKB1 در جلوگیری از التهاب در سلولها، نقش دارد؛ بهمین دلیل محققان به بررسی اینکه آیا SIK1 و SIK3 در مهار پاسخ التهاب سلولی در سلولهای سرطان ریه دخیل هستند، راغب شدند. زمانیکه LKB1 یا SIK1 و SIK3 در تومورها جهش مییابند، التهاب افزایش یافته و رشد تومور شدت مییابد.
اخیرا پروفسور مارک مونتمینی از انستیتو Salk در یک مطالعه، عوامل متابولیکی را که SIK1 و SIK3 در انتقال سیگنال، فعال میکنند، بررسی کرده و سه گامِ روندِ انتقالِ سیگنال توسط LKB1 را آشکار ساختهاند.
شاو میگوید: “با هجوم به مشکل سرطان ریه از تمامی زوایا، ما اکنون یک مسیر که چگونگی پیشرفت بیماری را در بسیاری از بیماران نشان میدهد، شناسایی کردهایم ما از سال ۲۰۰۶ بر روی این پروژه کار میکنیم و این مورد که التهاب یک نیروی پیشران در ایجاد تومور است، بسیار شگفت آور است. این کشف، طبیعتِ مطالعه علمی و اهمیت انجام آن بمنظور برطرف کردن مشکلات پیچیده را آشکار میسازد. حتی اگر ۱۰ سال برای رسیدن به پاسخ زمان نیاز باشد.” در گام بعدی، محققان بدنبال بررسی عوامل متابولیک کینازی در ایجاد التهاب که به رشد تومور در NSCLC منجر میشود، میباشد.
