توالی ژنوم انسان در سال ۲۰۰۱ منتشر شد، با این حال توالی DNA افراد مختلف به طور دقیق با آن مطابقت نمیکند و میلیونها چندشکلی (polymorphism) در ژنوم هر فرد وجود دارد. تحقیقات فراوانی بر روی تاثیر پلی مورفیسمها بر روی خصوصیات بیولوژیکی انجام شدهاست. با اینحال این موضوع همچنان به صورت چالشی در برابر دانشمندان قرار دارد، چون تاثیر ژنتیک بر رفتارها کاملا پیچیدهاست. مطالعات Yin و همکارانش به دانش ما در زمینه اساس ژنتیکی پیری افزودهاست. محققان با بررسی Caenorhabditis elegans که از کرمهای حلقوی است، دریافتند که تغییراتی که به طور طبیعی در دو ژن رخ میدهد، در زوال ناشی از پیری موثرند. آنان همچنین نشان دادند که این تغییرات، بر مسیرهایی را که فعالیت نورونها را کنترل میکنند، تاثیر میگذارند.
در ژنتیک کلاسیک، ژنهایی که رفتار موردنظر را تنظیم میکنند، از طریق بررسی تعداد زیادی جاندار که در معرض جهش قرار گرفتهاند، تعیین میشود؛ به گونهای که هر کدام دارای تغییر ژنتیکی متفاوتی هستند. این متد مدت زیادی است که در مدلهای آزمایشگاهی، برای تعیین تغییرات مخرب عامل غیرفعال شدن ژنها، به کار میرود. با این حال، تفاوتهای رفتاری بین افراد بیشتر تحت تاثیر تغییرات ژنتیکی فراوانی است که هر کدام تغییرات اندکی در بیان ژنها ایجاد میکنند (ژنتیک کلاسیک اینگونه رفتارها را بررسی نمیکند). این موضوع را میتوان تا حدودی به نیروهای تکاملی نسبت داد که جهشهای مخرب و دارای تاثیرات منفی فراوان را از جمعیت حذف میکنند.
مقاله مرتبط: کشف ژن ضد پیری
Caenorhabditis elegans، از آنجا که عمری کوتاه در حدود ۲ هفته دارد، اغلب در پژوهشهای مربوط به پیری مورد استفاده قرار میگیرد. Yin و همکارانش تفاوت میزان پیری را در گونههای وحشی این کرم مطالعه کردند که امکان بررسی تفاوتهایی را که به طور طبیعی در جمعیت رخ میدهند، فراهم میکند. محققان به جای طول عمر، میزان زوال ناشی از پیری را در فعالیتهایی همچون جفتیابی، تغذیه و تحرک اندازهگیری کردند.
پیشتر نشان دادهشدهبود که تغییر در بیان آنزیم BAS-1 با کاهش دو نوع عملکرد همراه است: جفت یابی و توانایی حلق در انتقال غذا از محیط به روده. در مطالعه فعلی، محققان تفاوتهای ژنتیکی را که بیان BAS-1 را تغییر میدهند، بررسی کردند. آنان همچنین پلی مورفیسمهایی را در یکی از ژنها شناسایی کردند که مسئول حدود نیمی از تفاوتهای زوال در این دو رفتار، ما بین نژادهای مختلف است. این ژن rgba-1 (regulatory gene for behavioral ageing-1) نامیده شد. محققان نشان دادند که جهشهایی که باعث از دست رفتن عملکرد rgba-1 میشوند، از زوال در فعالیتهای مربوط به جفتگیری جلوگیری میکنند.
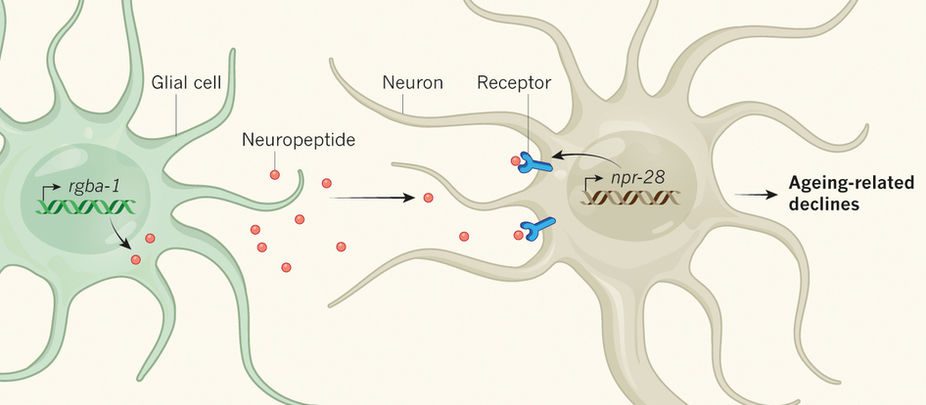
به نظر میرسد که rgba-1 منحصرا در C.elegans وجود داشته باشد و تاکنون حتی در گونههای مشابه کرمهای حلقوی مشاهده نشدهاست. این ژن حاوی رمزهای ژنتیکی ۴ نوروپپتید است. این نوروپپتیدها میتوانند به عنوان نوروترنسمیتر و یا نورومدولاتور عمل کنند. نوروترنسمیترها سیگنالها را بین نورونها منتقل میکنند و در سیناپسها آزاد میشوند. نورومدولاتورها وظیفه تنظیم اتصالات سیناپسی را بر عهده دارند و بسیار آهستهتر عمل میکنند. پس از انجام آزمایشات بسیار محققان NPR-28 را که رسپتور یکی از نوروپپتیدهای rgba-1 است (RGBA-1-2b)، شناسایی کردند. نوروپپتیدهای حاصل از rgba-1 مخصوص C.elegans هستند؛ اما NPR-28 اینگونه نیست. این رسپتور به رسپتورهای انسانی somatostatin و nociception مرتبط است و همانند آنها عملکرد نورونها را تنظیم میکند.
Yin و همکارانش پلیمورفیسمهایی در ژن NPR-28 مشاهده کردند که کاهش فعالیتهای جفتگیری در اثر افزایش سن را در نژادهای وحشی، تنظیم میکند. با این که پیری به صورت گستردهای در این کرم مطالعه شدهاست، متدهای ژنتیک کلاسیک، rgba-1 و npr-28 را به عنوان ژنهای درگیر در پیری شناسایی نکردهاند. این موضوع نشان میدهد که احتمالا مسیر این نوروپپتید به تفاوتهای ژنتیکی مرتبط باشد که تغییرات رفتاری جزئی ایجاد میکنند.
نورومدولاتورها وظیفه اصلی را در تنظیم فعالیت سیگنالهای نورونی دوربرد که بین نواحی مختلف مغز منتقل میشوند، دارند. از این رو بیان نوروپپتیدها و گیرندههای آنها راهی است که نیروهای تکاملی میتوانند از طریق آن رفتارها را بهینه کنند. ویژگیهای مربوط به پیری که rgba-1 و npr-28 آنها را تنظیم میکنند، تحت تاثیر انتخاب طبیعی نیستند. چون در سنین بالاتر و بعد از اینکه حداکثر تولید مثل رخ میدهد اثرات خود را بروز میدهند. این ژنها ممکن است بر خصوصیات جانوران جوانتر که تحت تاثیر نیروهای تکاملی هستند نیز تاثیر بگذارد. در حقیقت اثراتی که این ژنها بر پیری میگذارند ممکن است یک عارضه جانبی باشد.
نورومدولاتورها وظیفه اصلی را در تنظیم فعالیت سیگنالهای نورونی دوربرد بین نواحی مختلف مغز دارند. از این رو بیان نوروپپتیدها و گیرندههای آنها راهی است که نیروهای تکاملی میتوانند از طریق آن رفتارها را بهینه کنند. ویژگیهای مربوط به پیری که rgba-1 و npr-28 تنظیم میکنند، تحت تاثیر انتخاب طبیعی نیستند. چون در سنین بالاتر و بعد از اینکه حداکثر تولید مثل رخ میدهد اثرات خود را بروز میدهند. این ژنها ممکن است بر خصوصیات جانوران جوانتر که تحت تاثیر نیروهای تکاملی هستند نیز تاثیر بگذارد. در حقیقت اثراتی که این ژنها بر پیری میگذارند صرفا یک عارضه جانبی است.
مقاله مرتبط: نداشتن فعالیت بدنی، سرعت در پیری بیولوژیکی!
Yin و همکارانش احتمال میدادند که یک یا دو عدد از این نوروپپتیدها توسط سلولهای گلیال تولید شوند. سلولهای گلیال در پشتیبانی نورونها نقش دارند و نیز میتوانند مستقیما مدارهای نورونی را از طریق آزاد کردن سیگنالهایی تنظیم کنند. آنان در نهایت نشان دادند که npr-28 در نورونهایی بیان میشود که نوروترنسمیترهای سروتونین و دوپامین را ترشح میکنند. زمانی که گیرنده NPR-28 توسط نوروپپتید RGBA-1-2b فعال میشود، پاسخ استرسی یا mitochondrial unfolded protein response) mtUPR) را که در میتوکندری رخ میدهد، مهار میکند.
احتمالا آزاد شدن نوروپپتیدهای rgba-1 زمانی تحریک میشود که سلولهای گلیا تغییرات القا شده در اثر افزایش سن را در عملکرد نورونهایی که از آنها پشتیبانی میکنند، احساس کنند. این مکانیسم میتواند تحلیل ناشی از افزایش سن در عملکرد نورونها را با تغییرات مدارهای نورونی مرتبط کند. به عنوان مثال، کاهش میزان دوپامین در افراد مسن به علت مرگ نورونهای آزاد کننده دوپامین رخ میدهد. تصور میشود که این کاهش، در بروز علائم نورولوژیک پیری مانند از دست دادن تواناییهای شناختی و حافظه موثر است. احتمالا سیگنالهای نوروپپتیدی نیز در کاهش سطح دوپامین موثر باشند. افزایش فعالیت mtUPR میتواند این فرایند را به تاخیر بیندازد.
این مطالعه مکانیسمهای باارزشی را درمورد تاثیر تفاوتهای ژنتیکی بر زوال ناشی از افزایش سن ارائه میکند. چالش پیش رو این است که مشخص کنیم آیا این نوروپپتیدها تاثیر مشابهی در تنظیم طول عمر انسان دارند یا نه. تمرکز بر روی نوروپپتیدها و ارتباط آنها با پیری انسان میتواند به تولید داروهایی منجر شود که زوال ناشی از پیری را تا حدی بهبود میبخشند. با این وجود مکانیسمهای تنظیم کننده پیری بسیار پیچیدهتر از این نوروپپتیدها هستند. کشف این فرایندها میتواند باعث افزایش عمر مفید انسانها شود.